题目内容
下列说法不正确的是
| A.炔烃的官能团为-C≡C- | B.乙烯的结构简式为CH2CH2 |
| C.在铁制品上镀铜时用金属铜作阳极 | D.用Na2S做沉淀剂除去废水中的Cu2+和Hg2+ |
B
解析试题分析:A、炔烃分子中含有碳碳三键,因此炔烃官能团的结构式为-C≡C-,A正确;B、乙烯的结构简式为CH2=CH2,B不正确;C、电镀时待镀金属作阴极,与电源的负极相连。镀层金属作阳极,与电源的正极相连,所以在铁制品上镀铜时用金属铜作阳极,C正确;D、CuS与HgS都是不溶于水的沉淀,因此用Na2S做沉淀剂除去废水中的Cu2+和Hg2+,D正确,答案选B。
考点:考查考查官能团、乙烯结构简式、电镀以及溶解平衡的应用

练习册系列答案
相关题目
下列有机化学方程式书写错误的是
A.CH2=CH2 + HCl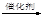 CH3CH2Cl CH3CH2Cl |
B.C12H22O11 + H2O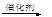 C6H12O6 + C6H12O6 C6H12O6 + C6H12O6蔗糖葡萄糖果糖 |
C.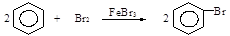 |
D.CH3COOH+CH3CH2OH 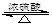 CH3COOCH2CH3+H2O CH3COOCH2CH3+H2O |
用NA代表阿伏加德罗常数,下列说法正确的是
| A.物质的量浓度为0.5mol/L的MgCl2溶液中,含有Cl-个数为1 NA |
| B.标准状况下,11.2 L H2O 所含的分子数为0.5NA |
| C.常温常压下,1.06g Na2CO3含有的Na+离子数为0.02 NA |
| D.18g H2O 和H2O2的混合物含有的分子数为1NA |
设NA为阿伏加德罗常数的数值,下列说法正确的是
| A.由2H和18O组成的水11 g,所含的中子数为4NA |
| B.标准状况下11.2 L乙烷和乙烯的混合气体中含有C原子数为NA |
| C.在0.1 mol·L-1的醋酸溶液中,所含H+的个数小于0.1NA |
| D.室温下H2O2分解得到16 g O2,转移的电子数为2NA |
Na、Mg、Al三种金属各2mol分别跟1L1mol?L-1的盐酸反应时,相同条件下放出氢气体积最大的是
| A.Al | B.Mg | C.Na | D.三者产生的氢气一样多 |
设NA为阿伏加德罗常数的值。下列说法正确的是
| A.常温下,pH=2的H2SO4溶液中含有的H+离子数目为0.01NA |
| B.当H2O与Na2O2反应生成1 molO2时,转移的电子数目为4NA |
| C.标准状况下,2.24 L CO和CO2混合气体中含有的碳原子数为0.1NA |
| D.1 L 0.1 mol·L-1 FeCl3溶液中含有的Fe3+离子数目为0.1NA |
设NA表示阿伏加德罗常数的值,下列表述不正确的是( )
| A.标准状况下,22.4L氢气所含原子数是2NA |
| B.5.4g水所含的分子数为0.3NA |
| C.含1mol硫酸钾的溶液中硫酸根离子数为2NA |
| D.1mol金属钠与水反应失去的电子数为NA |
NA表示阿伏加德罗常数,下列说法正确的是
| A.常温常压下,32g O2含有的原子数为2NA |
| B.100mL 1mol·L-1氨水中,含有OH- 离子数是0.1 NA |
| C.100mL 2 mol·L-1碳酸钠溶液中,CO2-3离子数为0.2NA |
| D.标准状况下,22.4LCl2通入足量NaOH溶液,转移的电子数为2NA |
在200 mL某硫酸盐溶液中,含有1.5NA个硫酸根离子(NA表示阿伏加德罗常数的值),同时含有NA个金属离子。则该硫酸盐的物质的量浓度为( )
| A.2 mol·L-1 | B.2.5 mol·L-1 | C.5 mol·L-1 | D.7.5 mol·L-1 |