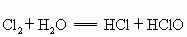题目内容
下列反应中,都有水参加,其中水既不作氧化剂又不作还原剂的氧化还原反应是( )
| A、钠投入水中:2Na+2H2O=2NaOH+H2↑ | B、氧化钠溶于水:Na2O+H2O=2NaOH | C、氯气溶于水:Cl2+H2O=HCl+HClO | D、氢化钠溶于水:NaH+H2O=NaOH+H2↑(NaH中H为-1价) |
分析:反应中含元素的化合价变化,为氧化还原反应,但水中H、O元素的化合价不变,则水既不作氧化剂又不作还原剂,以此来解答.
解答:解:A.Na元素的化合价升高,H元素的化合价降低,属于氧化还原反应,水为氧化剂,故A不选;
B.没有元素的化合价变化,不属于氧化还原反应,故B不选;
C.只有Cl元素的化合价变化,为水既不作氧化剂又不作还原剂的氧化还原反应,故C选;
D.NaH中H元素的化合价升高,水中H元素的化合价降低,属于氧化还原反应,水为氧化剂,故D不选;
故选C.
B.没有元素的化合价变化,不属于氧化还原反应,故B不选;
C.只有Cl元素的化合价变化,为水既不作氧化剂又不作还原剂的氧化还原反应,故C选;
D.NaH中H元素的化合价升高,水中H元素的化合价降低,属于氧化还原反应,水为氧化剂,故D不选;
故选C.
点评:本题考查氧化还原反应,为高考高频考点,把握反应中元素的化合价变化为解答的关键,侧重氧化还原反应判断的考查,题目难度不大.

练习册系列答案
 智慧小复习系列答案
智慧小复习系列答案
相关题目