题目内容
关于水的离子积常数Kw与水的电离平衡常数Kc的叙述中,正确的是( )A.Kw和Kc都随温度的升高而增大
B.Kw和Kc数值不同,但单位相同
C.Kw和Kc数值相同,但单位不同
D.Kw和Kc数值和单位都不同
【答案】分析:依据弱电解质的电离平衡常数只随温度的变化而变化,水的离子积是根据平衡常数计算得到的,也是只随温度变化,根据平衡常数的计算式和水的离子积的计算式比较分析判断;
解答:解析:A、由于水的电离是吸热的,所以升高温度,向电离程度增大的方向移动; H+和OH-浓度增大,故电离平衡常数Kc=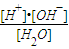 增大.而Kw=c(H+)?c(OH-),所以也增大,故A项正确.
增大.而Kw=c(H+)?c(OH-),所以也增大,故A项正确.
B、Kw的单位为mol2?L-2,Kc的单位为:mol?L-1,所以二者的单位不同;而Kw=Kc?[H2O],所以二者的数值也不同,故B错误;
C、Kw和Kc数值不相同,单位也不同,故C错误;
D、依据A的分析,Kw和Kc数值和单位都不同,故D正确;
故选AD.
点评:本题考查了水的离子积和平衡常数的计算式的应用和意义不同,关键是理解概念和应用.
解答:解析:A、由于水的电离是吸热的,所以升高温度,向电离程度增大的方向移动; H+和OH-浓度增大,故电离平衡常数Kc=
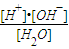 增大.而Kw=c(H+)?c(OH-),所以也增大,故A项正确.
增大.而Kw=c(H+)?c(OH-),所以也增大,故A项正确.B、Kw的单位为mol2?L-2,Kc的单位为:mol?L-1,所以二者的单位不同;而Kw=Kc?[H2O],所以二者的数值也不同,故B错误;
C、Kw和Kc数值不相同,单位也不同,故C错误;
D、依据A的分析,Kw和Kc数值和单位都不同,故D正确;
故选AD.
点评:本题考查了水的离子积和平衡常数的计算式的应用和意义不同,关键是理解概念和应用.

练习册系列答案
 优百分课时互动系列答案
优百分课时互动系列答案
相关题目
实验表明,相同温度下,液态纯硫酸的导电性强于纯水.下列关于相同温度下纯硫酸的离子积常数K和水的离子积常数Kw关系的描述正确的是( )
| A、K>Kw | B、K=Kw | C、K<Kw | D、无法比较 |
下列关于化学平衡常数(K),电离平衡常数(Ka或Kb),水解平衡常数(Kh),沉淀溶解平衡常数(Ksp),水的离子积常数(Kw)的叙述中错误的是( )
| A、K值越大,正反应进行的程度越大,一般地说,K>105时,该反应进行得就基本完全了 | B、比较Ksp与离子积Qc的相对大小,可判断难溶电解质在给定条件下沉淀能否生成或溶解 | C、K、Ka或Kb、Kh、Ksp、Kw都与温度有关,温度越高,常数值越大 | D、弱酸HA的Ka与NaA的Kh、水的离子积常数Kw三者间的关系可表示为:Kw=Ka?Kh |