题目内容
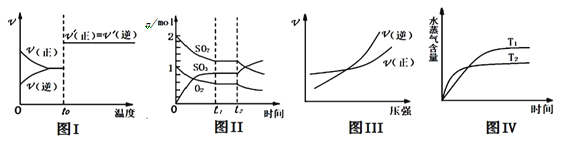
【题目】对可逆反应4NH3(g)+5O2(g)![]() 4NO(g)+6H2O(g),下列叙述正确的是
4NO(g)+6H2O(g),下列叙述正确的是
A. 若单位时间内生成xmolNO的同时,消耗xmolNH3,则反应达到平衡状态
B. 达到化学平衡时4v正(O2)=5v逆(NO)
C. 达到化学平衡时,若增大容器容积,则正反应速率减小,逆反应速率增大
D. 化学反应速率关系:2v正(NH3)=3v正(H2O)
【答案】B
【解析】若单位时间内生成xmolNO的同时,生成xmolNH3,则反应达到平衡状态,故A错误;正逆反应速率的比等于系数比时,一定平衡,故B正确;若增大容器容积,压强减小,则正逆反应速率均减小,故C错误;化学反应速率比等于系数比3v正(NH3)=2v正(H2O),故D错误。

 阅读快车系列答案
阅读快车系列答案【题目】硫酰氯(SO2C12)和氯化亚砜(SOC12)在空气中遇水蒸气发生剧烈反应,并产生大量白雾。硫酰氯(SO2C12)常用作氯化剂或氯磺化剂,用于制作药品、染料、表面活性剂等。合成的反应式为: SO2(g) + Cl2(g)![]() SO2Cl2(l) △H=-197.3 kJ·mol-1
SO2Cl2(l) △H=-197.3 kJ·mol-1
物质 | 熔点/℃ | 沸点/℃ | 其他性质 |
SO2C12 | -54.1 | 69.1 | 易分解:SO2C12 |
合成SO2C12的装置如下图所示(夹持仪器已省略),请回答有关问题:

(1)从下表中选择相应的装置完成填空:
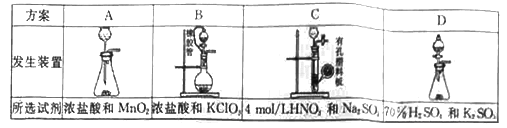
①制备SO2选________(填字母)。
②写出用所选装置制取Cl2的离子方程式_________________。
(2)合成SO2C12的装置图中仪器B的名称为_________________;丁中盛放的是_____________。
(3)反应结束后,将乙中混合物分离开的实验操作名称是 _______________。
(4)图中装置C的作用是__________________。
(5)为提高本实验中的产率,在实验操作中还需要注意的事项有(只答—条即可)__________。
(6)氯化亚砜(SOCl2)与水反应的化学方程式为_____,蒸干A1C13溶液不能得到无水AlCl3,用SOC12与AlCl3 6H2O的混合加热,可得到无水A1C13,试解释原因__________。
【题目】下列关于纯净物、混合物、强电解质、弱电解质和非电解质的正确组合是( )
纯净物 | 混合物 | 强电解质 | 弱电解质 | 非电解质 | |
(A) | 盐酸 | 水煤气 | 硫酸 | 醋酸 | 干冰 |
(B) | 冰醋酸 | 铝热剂 | 硫酸钡 | 亚硫酸 | 二氧化硫 |
(C) | 纯碱 | 天然气 | 苛性钾 | 氢硫酸 | 碳酸钙 |
(D) | 玻璃 | 盐酸 | 氯化钠 | 次氯酸 | 氯气 |
A. A B. B C. C D. D