题目内容
【题目】X、Y、Z、Q、R是五种短周期元素,原子序数依次增大。X、Y两元素最高正价与最低负价之和均为0;Q与X同主族;Z、R分别是地壳中含量最高的非金属元素和金属元素。
请回答下列问题:
(1)写出R的原子结构示意图:________________
(2)五种元素原子半径由大到小的顺序是(写元素符号) .
(3)X与Y能形成多种化合物其中既含极性键又含非极性键,且相对分子质量最小的物质是(写分子式) ,X和Z组成的化合物的化学式为___________________
(4)由以上某些元素组成的化合物A、B、C、D有如下转化关系:A![]() B(在水溶液中进行),其中,C是溶于水显酸性的气体;D是淡黄色固体。写出C的化学式 ;D的电子式 .
B(在水溶液中进行),其中,C是溶于水显酸性的气体;D是淡黄色固体。写出C的化学式 ;D的电子式 .
①如果A、B均由三种元素组成,B为两性不溶物,则A![]() B离子反应方程式为_________
B离子反应方程式为_________
②A、B均为盐溶液,如果A由三种元素组成,B由四种元素组成,A、B溶液均显碱性.用离子方程式表示A溶液显碱性的原因 ;常温下,在该溶液中滴加稀盐酸至中性时,溶质的主要成分有 .
【答案】(1)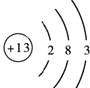 ;
;
(2)Na>Al>C>O>H
(3)C2H2; H2O和H2O2 ;
(4)CO2;![]() ;
;
①AlO2-+CO2+2H2O==Al(OH)3↓+HCO3-;②CO32-+H2O![]() HCO3-+OH-;NaCl H2CO3NaHCO3
HCO3-+OH-;NaCl H2CO3NaHCO3
【解析】试题分析:X、Y、Z、Q、R是五种短周期元素,原子序数依次增大,Z、R分别是地壳中含量最高的非金属元素和金属元素,则Z为O元素、R为Al;X、Y两元素最高正价与最低负价代数和均为0,原子序数均小于O元素,为ⅠA族元素、ⅣA族元素,故X为H元素、Y为C元素;Q与X同主族,结合原子序数可知,Q为Na元素。
(1)R为Al,原子结构示意图为 ,故答案为:
,故答案为: ;
;
(2)同周期自左而右原子半径减小,电子层越多原子半径越大,故原子半径Na>Al>C>O>H,故答案为:Na>Al>C>O>H;
(3)H与C形成多种化合物,属于烃类物质,其中既含极性键又含非极性键,且相对分子质量最小是C2H2,H与O形成的化合物有H2O和H2O2,故答案为:C2H2;H2O和H2O2;
(4)由以上某些元素组成的化合物A、B、C、D有如下转化关系:A![]() B(在水溶液中进行),其中,C是溶于水显酸性的气体;D是淡黄色固体。则D是Na2O2,C是CO2,D的电子式为
B(在水溶液中进行),其中,C是溶于水显酸性的气体;D是淡黄色固体。则D是Na2O2,C是CO2,D的电子式为![]() ,故答案为:CO2;
,故答案为:CO2;![]() ;
;
①如果A、B均由三种元素组成,B为两性不溶物,则B是Al(OH)3,D是过氧化钠、C是二氧化碳,则A是偏铝酸钠,其化学式为NaAlO2,偏铝酸钠和过量二氧化碳反应生成氢氧化铝和碳酸氢根离子,离子反应方程式为:AlO2-+2H2O+CO2=Al(OH)3+HCO3-,故答案为:AlO2-+2H2O+CO2=Al(OH)3+HCO3-;
②如果A由三种元素组成,B由四种元素组成,A、B溶液均显碱性,B和氢氧化钠反应生成A,A和二氧化碳反应生成B,所以B是碳酸氢钠、A是碳酸钠,碳酸根离子水解导致碳酸钠溶液呈碱性,水解方程式为CO32-+H2O![]() HCO3-+OH-;常温下,A、B浓度均为0.1molL-1的混合溶液中,滴加盐酸,生成NaCl,但溶液中溶解二氧化碳,溶液呈中性时,应有部分NaHCO3,则溶液中的溶质为NaHCO3、NaCl、CO2或者碳酸,故答案为:CO32-+H2O
HCO3-+OH-;常温下,A、B浓度均为0.1molL-1的混合溶液中,滴加盐酸,生成NaCl,但溶液中溶解二氧化碳,溶液呈中性时,应有部分NaHCO3,则溶液中的溶质为NaHCO3、NaCl、CO2或者碳酸,故答案为:CO32-+H2O![]() HCO3-+OH-; NaHCO3、NaCl、CO2或者碳酸
HCO3-+OH-; NaHCO3、NaCl、CO2或者碳酸

 海淀黄冈名师导航系列答案
海淀黄冈名师导航系列答案 普通高中同步练习册系列答案
普通高中同步练习册系列答案【题目】研究CO2的利用对促进低碳社会的构建具有重要的意义。
(1)将CO2与焦炭作用生成CO,CO可用于炼铁等。
已知:Fe2O3(s)+3C(石墨)=2Fe(s)+3CO(g) ΔH1=+489.0 kJ·mol-1
C(石墨)+CO2(g)=2CO(g) ΔH2=+172.5 kJ·mol-1
则CO还原Fe2O3的热化学方程式为___________________________
(2)某实验将CO2和H2充入一定体积的密闭容器中,在两种不同温度条件下反应:
CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) ΔH=-49.0 kJ·mol-1
CH3OH(g)+H2O(g) ΔH=-49.0 kJ·mol-1
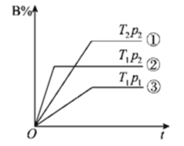
测得CH3OH的物质的量随时间变化如图所示,回答问题:
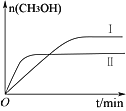
①该反应的平衡常数表达式K=_______________;
②曲线Ⅰ、Ⅱ对应的平衡常数大小关系为:KⅠ_________KⅡ(填“>”、“=”或“<”)。
③下列措施中能增大CO2转化率的是____________。(填序号)
A.升高温度 | B.充入He(g)使体系压强增大 |
C.将H2O(g)从体系中分离 | D.再充入一定量CO2 |
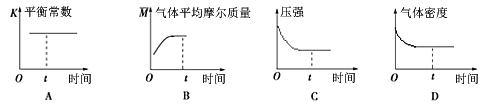
④下列图像正确且能表明在t时刻反应一定处于平衡状态的是__________。(填序号)