题目内容
【题目】四氧化三铁(Fe3O4)磁性纳米颗粒稳定、容易生产且用途广泛,是临床诊断、生物技术和环境化学领域多种潜在应用的有力工具。水热法制备Fe3O4纳米颗粒的反应是3Fe2++2S2O![]() +O2+xOH-=Fe3O4↓+S4O
+O2+xOH-=Fe3O4↓+S4O![]() +2H2O。请回答下列问题。
+2H2O。请回答下列问题。
(1)水热法制备Fe3O4纳米颗粒的反应中,还原剂是____________。
(2)反应的化学方程式中x=________。
(3)每生成1 mol Fe3O4,反应转移的电子为________mol,被Fe2+还原的O2的物质的量为________mol。
【答案】 Fe2+、S2O32- 4 4 0.5
【解析】(1)反应中Fe元素化合价部分升高为+3价,S元素化合价由+2价升高到+2.5价,则还原剂是Fe2+和S2O32-,故答案为:Fe2+和S2O32-;
(2)由电荷守恒可知,(+2)×3+(-2)×2+x×(-1)=-2,则x=4,故答案为:4;
(3)Fe、S元素的化合价升高,O元素的化合价降低,由反应可知,该反应转移4e-,所以每生成1mol Fe3O4,由O元素的化合价变化可知,转移电子为1mol×2×[0-(-2)]=4mol,每生成1mol Fe3O4,消耗3molFe2+,其中有2molFe2+被氧化生成+3价,则被Fe2+还原的O2的物质的量为![]() mol=0.5mol,故答案为:4;0.5。
mol=0.5mol,故答案为:4;0.5。

 快捷英语周周练系列答案
快捷英语周周练系列答案【题目】蛇纹石矿可以看作由MgO、Fe2O3、Al2O3、SiO2组成。由蛇纹石制取碱式碳酸镁的实验步骤如下图所示:
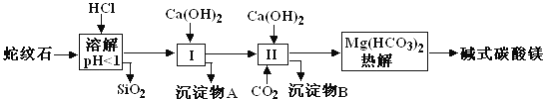
(1)蛇纹石加盐酸溶解后,溶液里除了Mg2+外,还含有的金属离子是__________。
(2)进行Ⅰ操作时,控制溶液pH=7~8(有关氢氧化物沉淀的pH见下表)。
氢氧化物 | Fe(OH)3 | Al(OH)3 | Mg(OH)2 |
开始沉淀pH | 1.5 | 3.3 | 9.4 |
Ca(OH)2不能过量,若Ca(OH)2过量可能会导致__________溶解、________沉淀。
(3)从沉淀混合物A中提取红色氧化物作颜料,先向沉淀物A中加入__________(填写物质的化学式),然后过滤、洗涤、灼烧。
(4)现设计一个实验,确定产品aMgCO3bMg(OH)2cH2O中a、b、c的值,请完善下列实验步骤(可用试剂:浓硫酸、碱石灰):
①样品称量 ②高温分解
③ ______________________________________________________。
④称量碱石灰吸收CO2前后的质量 ⑤MgO称量
(5)18.2 g产品完全分解后,产生6.6 g CO2和8.0 g MgO,由此可知,产品的化学式中:a=____________,b=____________,c=____________。
