题目内容
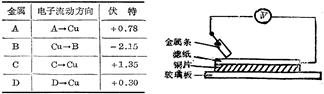
如图示实验中,把四根洁净的金属条A、B、C、D轮流放置在浸有盐溶液的滤纸上面并压紧.在每次轮流实验时,记录了电压表指针的移动方向和电压表的读数(如右表).

(1)
(2)

(1)
C
C
金属可能是最强的还原剂;(2)
B
B
金属不能从硫酸铜溶液中置换铜.分析:根据电子的流向判断电极材料与铜的金属性强弱;根据电压表的度数判断A、C、D的金属性强弱.
解答:解:A-Cu连接时,电子从A→Cu,所以A的金属性大于铜;
B--Cu连接时,电子从Cu→B,所以铜的金属性大于B;
C--Cu连接时,电子从C→Cu,所以C的金属性大于铜;
D--Cu连接时,电子从D→Cu,所以D的金属性大于铜;
(1)金属的金属性越强,电压表的读数越大,连接 C--Cu时,电压表的读数最大,所以C的金属性最强,其还原性最强;
故答案为:C.
(2)根据上面分析知,铜的金属性大于B,所以B金属不能从硫酸铜溶液中置换铜.
故答案为:B.
B--Cu连接时,电子从Cu→B,所以铜的金属性大于B;
C--Cu连接时,电子从C→Cu,所以C的金属性大于铜;
D--Cu连接时,电子从D→Cu,所以D的金属性大于铜;
(1)金属的金属性越强,电压表的读数越大,连接 C--Cu时,电压表的读数最大,所以C的金属性最强,其还原性最强;
故答案为:C.
(2)根据上面分析知,铜的金属性大于B,所以B金属不能从硫酸铜溶液中置换铜.
故答案为:B.
点评:本题以原电池原理为载体考查了金属的金属性强弱比较,在原电池中可根据电子的流向、电极反应的反应类型、电极材料的变化等方法判断金属的金属性强弱,但不可根据电极的正负极判断金属的金属性强弱.

练习册系列答案
相关题目