题目内容
下列反应的离子方程式书写中,正确的是
| A.小苏打溶液中加入少量NaOH溶液: H ++ OH-=H2O |
| B.铁跟稀硫酸反应:2Fe+6H+=2Fe3++3H2↑ |
| C.硫酸铜溶液与氢氧化钡溶液混合:Cu2+ + 2OH—=Cu(OH)2↓ |
| D.氧化铁与稀硫酸反应:Fe2O3 + 6H+=2Fe3+ + 3H2O |
D
解析试题分析:A、小苏打溶液中加入少量NaOH溶液生成碳酸钠和水,反应的离子方程式为HCO3-+ OH-=CO32-+H2O,A不正确;B、铁与稀硫酸反应生成硫酸亚铁和氢气,反应的离子方程式为Fe+2H+=Fe2++H2↑,B不正确;C、硫酸铜溶液与氢氧化钡溶液混合生成硫酸钡和氢氧化铜沉淀,所以反应的离子方程式为SO42-+Cu2+ +Ba2++ 2OH—=Cu(OH)2↓+BaSO4↓,C不正确;D、氧化铁与稀硫酸反应生成硫酸铁和水,所以离子方程式为Fe2O3 + 6H+=2Fe3+ + 3H2O,D正确,答案选D。
考点:考查离子方程式的正误判断

练习册系列答案
 优加精卷系列答案
优加精卷系列答案
相关题目
下物质分类组合正确的是 ( )
| | A | B | C | D |
| 强电解质 | HBr | FeCl3 | H3PO4 | Ca(OH)2 |
| 弱电解质 | HF | CH3COOH | BaSO4 | HI |
| 非电解质 | NH3 | Cu | H2O | C2H5OH |
下列关于强、弱电解质的叙述,有错误的是
| A.强电解质在溶液中完全电离,不存在电离平衡 |
| B.在溶液中,导电能力强的电解质是强电解质,导电能力弱的电解质是弱电解质 |
| C.强电解质都是离子化合物,弱电解质都是共价化合物 |
| D.纯净的强电解质在液态时,有的导电,有的不导电 |
在含有较多Ba2+、NO3ˉ、Clˉ的溶液中还能大量共存的离子是
| A.Ag+ | B.Mg2+ | C.SO42ˉ | D.CO32一 |
下列物质在水溶液中的电离方程式正确的是( )。
| A.NaHSO4=Na++H++SO42— | B.KClO3=K++Cl5++3O2— |
| C.Ba(OH)2=Ba2++(OH)22— | D.H2SO4=H2++SO42— |
下列状态的物质,既能导电又属于电解质的是
| A.MgCl2晶体 | B.熔融的NaCl | C.液态酒精 | D.KOH溶液 |
下列离子方程式正确的是( )
| A.钠与水反应:Na + 2H2O = Na++ 2OH-+ H2↑ |
| B.硅酸钠溶液与醋酸溶液混合:SiO32-+ 2H+ = H2SiO3↓ |
| C.0.01mol/LNH4Al(SO4)2溶液与0.02mol/LBa(OH)2溶液等体积混合: NH4++Al3++ 2SO42-+ 2Ba2++ 4OH- = 2BaSO4↓ + Al(OH)3↓ + NH3·H2O |
| D.浓硝酸中加入过量铁粉并加热:Fe + 3NO3-+ 6H+ =Fe3+ + 3NO2↑ + 3H2O |
下列相关反应的离子方程式书写正确的是
| A.浓盐酸与铁屑反应:2Fe+6H+=2Fe3++3H2↑ |
| B.钠与硫酸铜溶液反应:2Na+Cu2+==Cu+2Na+ |
| C.向硫酸铝溶液中加入过量氨水:Al3+ + 3OH-=Al(OH)3↓ |
| D.将铜片放入足量稀硝酸中:3Cu + 8H++ 2NO3- = 3Cu2+ + 2NO↑+ 4H2O |
常温下,下列各组离子在指定溶液中一定能大量共存的是
A.强酸性溶液中:Mg2+、K+、SO42-、NO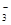 |
B.强碱性溶液中:Na+、Cu2+、HCO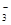 、NO 、NO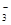 |
| C.0.1mol·L-1AgNO3溶液中:H+、K+、SO42-、Cl- |
| D.0.1mol·L-1Ba(NO3)2溶液:Mg2+、K+、SO42-、Cl- |