题目内容
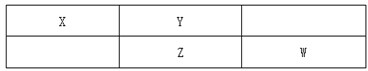
短周期元素X、Y、Z、W在元素周期表中的位置关系如图.若Y原子的最外层电子数是内层电子数的3倍,则下列说法正确的是( )

| A、原子半径:W>Z>Y>X |
| B、最高价氧化物对应水化物的酸性:Z>W>X |
| C、Y可形成的氢化物中有一种式量与Z的氢化物式量相同 |
| D、四种元素的单质中,W单质的熔沸点最高 |
考点:元素周期律和元素周期表的综合应用
专题:元素周期律与元素周期表专题
分析:短周期元素X、Y、Z、W,Y原子的最外层电子数是内层电子数的3倍,Y原子只能有2个电子层,最外层电子数为6,则Y为O元素,由元素在周期表中的位置可知,X为N元素、Z为S元素、W为Cl,据此解答.
解答:
解:短周期元素X、Y、Z、W,Y原子的最外层电子数是内层电子数的3倍,Y原子只能有2个电子层,最外层电子数为6,则Y为O元素,由元素在周期表中的位置可知,X为N元素、Z为S元素、W为Cl,
A.同周期自左而右原子半径减小,电子层越多原子半径越大,故原子半径:Z>W>X>Y,故A错误;
B.同周期自左而右元素非金属性减弱,非金属性Z<W,故最高价氧化物对应水化物的酸性:Z<W,故B错误;
C.Y形成的氢化物H2O2与Z的氢化物H2S的式量相等,故C正确;
D.四种元素的单质中,常温下,硫单质为固体,其它三种单质为气体,故硫单质的熔沸点最高,故D错误,
故选C.
A.同周期自左而右原子半径减小,电子层越多原子半径越大,故原子半径:Z>W>X>Y,故A错误;
B.同周期自左而右元素非金属性减弱,非金属性Z<W,故最高价氧化物对应水化物的酸性:Z<W,故B错误;
C.Y形成的氢化物H2O2与Z的氢化物H2S的式量相等,故C正确;
D.四种元素的单质中,常温下,硫单质为固体,其它三种单质为气体,故硫单质的熔沸点最高,故D错误,
故选C.
点评:本题考查结构性质位置关系应用,难度不大,推断元素是解题关键,注意对元素周期表的把握及对元素周期律的理解掌握.

练习册系列答案
 字词句段篇系列答案
字词句段篇系列答案
相关题目
下列说法错误的是( )
| A、s轨道呈圆形,p轨道呈哑铃形 |
| B、Cr元素在元素周期表的d区 |
| C、焰色反应是因为电子跃迁产生的 |
| D、DNA中的碱基互补配对是通过氢键来实现的 |
短周期主族元素X、Y、Z、W的原子序数依次增大,X原子核外最外层电子数是次外层的2倍,Y的氟化物YF3分子中各原子均达到8电子稳定结构,Z是同周期中原子半径最大的元素,W的最高正价为+7价.下列说法正确的是( )
| A、XH4的沸点比YH3高 |
| B、X与W形成的化合物和Z与W形成的化合物的化学键类型相同 |
| C、元素W的最高价氧化物对应水化物的酸性比Y的强 |
| D、X与Y形成的化合物的熔点可能比金刚石高 |
下列说法正确的是( )
| A、互为手性的分子具有相似的性质,故生产药物时不必分离 |
| B、NF3分子立体构型为三角锥形,是极性分子 |
| C、N2O和CO2互为等电子体所以化学性质相似 |
| D、酸性:HClO>HClO2>HClO3>HClO4 |
下列各项反应对应的图象错误的是( )
A、 将饱和FeCl3溶液滴入沸水中制备Fe(OH)3胶体 |
B、 将稀盐酸逐滴加入一定量偏铝酸钠溶液中 |
C、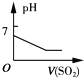 将二氧化硫逐渐通入一定量氯水中 |
D、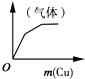 将铜粉逐渐加入一定量浓硝酸中 |
1.1mol氯气跟白磷完全反应生成三氯化磷和五氯化磷,其物质的量比为2:1,则生成物中五氯化磷的物质的量为( )
| A、0.4mol |
| B、0.1mol |
| C、0.2mol |
| D、0.05mol |
下列物质的性质,用途正确的是( )
| A、浓硫酸、浓硝酸都具有强氧化性,不能盛放在金属容器内 |
| B、二氧化碳、二氧化硅都是酸性氧化物,均能与水反应生成相应的酸 |
| C、明矾、漂白粉常用于自来水净化,均利用了物质的强氧化性 |
| D、铝、氧化铝、氢氧化铝、碳酸氢钠既能与强酸反应又能与强碱反应 |
在标准状况下,气体A的密度为1.25g/L,气体B的密度为1.875g/L,A和B的混合气体在相同状况下对氢气的相对密度为16.8,则混合气体中A与B的体积比为( )
| A、1:2 | B、2:1 |
| C、2:3 | D、3:2 |