题目内容
【题目】按要求对如图中两极进行必要的联接并填空:
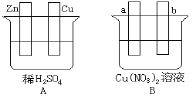
(1)在A图中,使铜片上冒H2气泡。请加以必要联接___,则联接后的装置叫___。电极反应式:锌板:___;铜板:___。
(2)在B图中(a、b均为惰性电极),使a极析出铜,则b析出:___。加以必要的联接后,该装置叫___。电极反应式,a极:___,b极:___。经过一段时间后,停止反应并搅均溶液,溶液的pH值___(升高、降低、不变),加入一定量的___后,溶液能恢复至与电解前完全一致。
【答案】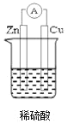 原电池 Zn-2e-=Zn2+ 2H++2e-=H2↑ O2 电解池 Cu2++2e-=Cu 2H2O4e=O2↑+4H+ 降低 CuO或者CuCO3
原电池 Zn-2e-=Zn2+ 2H++2e-=H2↑ O2 电解池 Cu2++2e-=Cu 2H2O4e=O2↑+4H+ 降低 CuO或者CuCO3
【解析】
(1)在A图中,使铜片上冒H2气泡,该装置必须形成闭合回路,该装置应该为原电池,且Cu作正极,Zn作负极,负极上锌失电子生成锌离子,正极上氢离子得电子生成氢气;
(2)在B图中(a、b均为惰性电极),使a极析出铜,该装置应该是电解池,a电极上铜离子放电生成Cu,b电极上水电离的氢氧根离子失电子生成氧气,且b电极有H+生成导致溶液pH降低,要使混合溶液恢复原状,根据“析出什么加入什么”的原则判断加入物质。
(1)要使该装置中Cu片上生成氢气,必须形成闭合回路,该装置应为原电池,装置图如图所示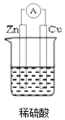 ,Zn作负极、Cu作正极,负极反应式为Zn2e=Zn2+、正极反应式为2H++2e=H2↑;
,Zn作负极、Cu作正极,负极反应式为Zn2e=Zn2+、正极反应式为2H++2e=H2↑;
故答案为: ;原电池;Zn2e=Zn2+;2H++2e=H2↑;
;原电池;Zn2e=Zn2+;2H++2e=H2↑;
(2)B图中(a、b均为惰性电极),使a极析出铜,a电极上铜离子放电生成Cu,该装置应为电解池,则b电极上H2O电离的氢氧根离子失电子生成氧气,所以析出O2,a、b电极反应式分别为Cu2++2e=Cu、2H2O4e=O2↑+4H+,有氢离子生成导致溶液pH减小,实际上相当于析出CuO,要使混合溶液恢复原状,应该加入CuO或者CuCO3;
故答案为:O2;电解池;Cu2++2e=Cu;2H2O4e=O2↑+4H+;降低;CuO或者CuCO3。

【题目】仅用下表提供的仪器![]() 夹持仪器和试剂任选
夹持仪器和试剂任选![]() 不能达到相应实验目的一组是
不能达到相应实验目的一组是
选项 | 实验目的 | 仪器 |
A | 用CCl4提取溴水中的溴单质 | 烧杯、玻璃棒、分液漏斗 |
B | 从食盐水中获得NaCl晶体 | 酒精灯、玻璃棒、坩埚、泥三角 |
C | 配制100mL1.0mol/L的NaOH溶液 | 药匙、天平、量筒、烧杯、玻璃棒、胶头滴管、100mL的容量瓶 |
D | 用盐酸除去BaSO4中混有少量BaCO3 | 漏斗、烧杯、玻璃棒、胶头滴管、滤纸 |
A. B. C. D.
【题目】下列实验中,对应的现象以及结论均正确的是( )
选项 | 实验操作 | 实验现象 | 结论 |
A | 取少量Na2SO3固体于试管中,加水溶解,滴加Ba(NO3)2溶液,再滴加稀硝酸 | 滴加Ba(NO3)2溶液,产生白色沉淀,再滴加稀硝酸,沉淀不溶解 | Na2SO3固体已经变质 |
B | 将SO2通入酸性KMnO4溶液中 | 溶液的紫红色褪去 | SO2具有漂白性 |
C | 将铁片投入浓硫酸中 | 无明显变化 | 常温下铁不与浓硫酸反应 |
D | 将10mL2mol/L的KI溶液与1mL1mol/LFeCl3溶液混合充分反应后滴加KSCN溶液 | 溶液颜色变红 | KI与FeCl3的反应具有可逆性 |
A.AB.BC.CD.D