题目内容
下列化工生产原理错误的是( )
①可以电解熔融的氯化钠来制取金属钠;②可以将钠加入氯化镁饱和溶液中制取镁;③用电解法冶炼铝时,原料是氯化铝;④高炉炼铁的反应是放热的,故无需加热
| A.②③ | B.①③ |
| C.①②③ | D.②③④ |
D
解析

练习册系列答案
 轻松夺冠全能掌控卷系列答案
轻松夺冠全能掌控卷系列答案
相关题目
下列叙述正确的是( )
| A.工业上用电解熔融氯化钠的方法制取钠 |
| B.钠加入氯化镁的饱和溶液中可以制取金属镁 |
| C.电解冶炼铝的原料是氯化铝 |
| D.电解氯化镁溶液来制取镁 |
下列金属冶炼的反应原理,错误的是 ( )
A.2NaCl(熔融) 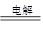 2 Na+Cl2↑ 2 Na+Cl2↑ | B.MgO+H2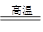 Mg+H2O Mg+H2O |
C.Fe2O3+3CO 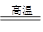 2Fe+3CO2 2Fe+3CO2 | D.2HgO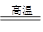 2Hg+O2↑ 2Hg+O2↑ |
离子膜法制烧碱示意图如下图所示,有关说法正确的是 ( )。
| A.a口进水 |
| B.b口进精制饱和食盐水 |
| C.c口出的是Cl-,是由b口进入的 |
| D.d口出的是H2 |
天然海水中主要含有Na+、K+,Ca2+、Mg2+、Cl-、SO42—、Br-、CO32—、HCO3—等离子,火力发电燃煤排放的含SO2的烟气可利用海水脱硫,其工艺流程如下图所示:
下列说法错误的是 ( )
| A.天然海水pH≈8的原因是海水中的CO32—、HCO3—水解 |
| B.“氧化”是利用氧气将H2SO3、HSO3—、SO32—等氧化生成SO42— |
| C.“反应、稀释”时加天然海水的目的是中和、稀释经氧气氧化后海水中生成的酸 |
| D.“排放”出来的海水中SO42—的物质的量浓度与进入吸收塔的天然海水相同 |
许多国家十分重视海水资源的综合利用,不需要化学变化就能从海水中获得的物质是( )。
| A.Cl2、Br2、I2 | B.Na、Mg、Al |
| C.食盐、淡水 | D.NaOH、H2 |
下列元素①Cl、②Na、③Br、④I、⑤Mg、⑥U,属于海水中的微量元素的是( )
| A.①②⑤ | B.④⑥ |
| C.①②③④ | D.③④⑤⑥ |
下列制备金属单质的方法或原理正确的是( )
| A.在高温条件下,用H2还原MgO制备单质Mg |
| B.在通电条件下,电解熔融Al2O3制备单质Al |
| C.在通电条件下,电解饱和食盐水制备单质Na |
| D.加强热,使CuO在高温条件下分解制备单质Cu |