题目内容
五种短周期元素在周期表中的相对位置如下所示,其中Z元素原子核外电子总数是其最外层电子数的3倍。
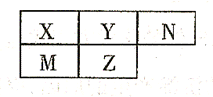
请回答下列问题:
(1)元素X位于周期表中第 周期, 族;
(2)这些元素的氢化物中,稳定性最强的是 (写化学式);
(3)Y与N形成的化合物中,Y可能的化合价有 ;
(4)M、Z的原子半径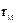
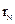 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。

请回答下列问题:
(1)元素X位于周期表中第 周期, 族;
(2)这些元素的氢化物中,稳定性最强的是 (写化学式);
(3)Y与N形成的化合物中,Y可能的化合价有 ;
(4)M、Z的原子半径
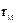
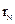 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。(1)二(1分),ⅥA族(1分)
(2)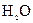 (1分)
(1分)
(3)+1+2+3+4+5(2分)
(4)>(1分)
(2)
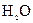 (1分)
(1分) (3)+1+2+3+4+5(2分)
(4)>(1分)
略

练习册系列答案
相关题目

 。
。 个σ键, 个π键。
个σ键, 个π键。
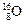 、
、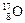 、
、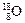 三种核素,氢元素有
三种核素,氢元素有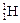 、
、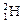 、
、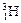 三种核素。
三种核素。 分子
分子  性
性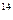
 C含量,能测出古代物品所处的年代。
C含量,能测出古代物品所处的年代。