题目内容
露置于空气中一段时间后的水玻璃会浑浊.向此浑浊溶液中加入稀盐酸,会生成白色沉淀,同时伴随有气泡产生.用化学方程式解释产生上述现象的原因:(1)溶液变浑浊:
(2)生成白色沉淀:
(3)产生气泡:
分析:(1)水玻璃是硅酸钠的水溶液,碳酸的酸性强于硅酸,所以水玻璃能与空气中二氧化碳反应生成硅酸沉淀;
(2)盐酸是强酸,硅酸是弱酸,水玻璃是强碱弱酸盐,所以盐酸能和硅酸钠反应生成硅酸沉淀;
(3)露置于空气中一段时间后的水玻璃和空气中的二氧化碳反应生成硅酸沉淀的同时生成碳酸钠,碳酸钠和盐酸反应有二氧化碳生成;
(2)盐酸是强酸,硅酸是弱酸,水玻璃是强碱弱酸盐,所以盐酸能和硅酸钠反应生成硅酸沉淀;
(3)露置于空气中一段时间后的水玻璃和空气中的二氧化碳反应生成硅酸沉淀的同时生成碳酸钠,碳酸钠和盐酸反应有二氧化碳生成;
解答:(1)空气中有二氧化碳,二氧化碳和水反应生成碳酸,碳酸的酸性强于硅酸,根据强酸制弱酸,水玻璃能与空气中二氧化碳反应生成硅酸沉淀,
反应为Na2SiO3+CO2+H2O=H2SiO3↓+Na2CO3,
故答案为:Na2SiO3+CO2+H2O=H2SiO3↓+Na2CO3;
(2)置于空气中一段时间后的水玻璃会浑浊,但此时出现的硅酸沉淀的量较少,向此浑浊溶液中加入稀盐酸,盐酸是强酸,硅酸是弱酸,所以盐酸能和浑浊溶液中的硅酸钠反应生成硅酸沉淀,反应为:Na2SiO3+2HCl=H2SiO3↓+2NaCl,
故答案为:Na2SiO3+2HCl=H2SiO3↓+2NaCl;
(3)因盐酸的酸性强于碳酸,碳酸的酸性强于硅酸,所以露置于空气中一段时间后的水玻璃和空气中的二氧化碳反应生成硅酸沉淀的同时生成碳酸钠,当向该混合物中滴加盐酸,盐酸先和剩余的硅酸钠反应,假设先和碳酸钠反应,那反应生成的二氧化碳还是和硅酸钠反应生成硅酸和碳酸钠,所以假设不成立,应为当向此浑浊溶液中滴加盐酸,先发生Na2SiO3+2HCl=H2SiO3↓+2NaCl,后发生Na2CO3+2HCl=2NaCl+CO2↑+H2O,
故答案为:Na2CO3+2HCl=2NaCl+CO2↑+H2O;
反应为Na2SiO3+CO2+H2O=H2SiO3↓+Na2CO3,
故答案为:Na2SiO3+CO2+H2O=H2SiO3↓+Na2CO3;
(2)置于空气中一段时间后的水玻璃会浑浊,但此时出现的硅酸沉淀的量较少,向此浑浊溶液中加入稀盐酸,盐酸是强酸,硅酸是弱酸,所以盐酸能和浑浊溶液中的硅酸钠反应生成硅酸沉淀,反应为:Na2SiO3+2HCl=H2SiO3↓+2NaCl,
故答案为:Na2SiO3+2HCl=H2SiO3↓+2NaCl;
(3)因盐酸的酸性强于碳酸,碳酸的酸性强于硅酸,所以露置于空气中一段时间后的水玻璃和空气中的二氧化碳反应生成硅酸沉淀的同时生成碳酸钠,当向该混合物中滴加盐酸,盐酸先和剩余的硅酸钠反应,假设先和碳酸钠反应,那反应生成的二氧化碳还是和硅酸钠反应生成硅酸和碳酸钠,所以假设不成立,应为当向此浑浊溶液中滴加盐酸,先发生Na2SiO3+2HCl=H2SiO3↓+2NaCl,后发生Na2CO3+2HCl=2NaCl+CO2↑+H2O,
故答案为:Na2CO3+2HCl=2NaCl+CO2↑+H2O;
点评:本题主要考查了硅酸的制取,明确盐酸的酸性强于碳酸,碳酸的酸性强于硅酸是解答本题的关键,题目难度不大.

练习册系列答案
 优等生题库系列答案
优等生题库系列答案
相关题目
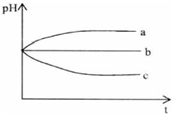 (2012?上饶一模)将pH相同的三种酸性溶液露置于空气中一段时间后,溶液的pH随时间的变化情况如图所示:则a、b、c三种溶液分别可能为( )
(2012?上饶一模)将pH相同的三种酸性溶液露置于空气中一段时间后,溶液的pH随时间的变化情况如图所示:则a、b、c三种溶液分别可能为( )