题目内容
【题目】2molA与2molB混合于2L的密闭容器中,发生如下反应:2A(g)+3B(g)![]() 2C(g)+zD(g),2s末A的转化率为50%,测得v(D)=0.25molL﹣1s﹣1,下列推断不正确的是
2C(g)+zD(g),2s末A的转化率为50%,测得v(D)=0.25molL﹣1s﹣1,下列推断不正确的是
A. 2s末,B的浓度为0.5mol/L B. 2s末,容器内的压强是初始的7/8倍
C. 2s时C的体积分数为2/7 D. z=2
【答案】A
【解析】A的初始物质的量为2mol,2s末A的转化率为50%,则A反应了1mol,由化学方程式可得,A、B按2:3的物质的量之比反应,所以B反应了1.5mol;v(D)=0.25molL﹣1s﹣1,则D生成了0.25molL﹣1s﹣1×2s×2L=1mol,由题意列三段式:
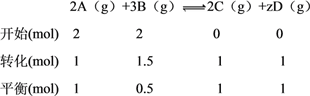
A项,2s末,反应物B的浓度为:0.5mol÷2L=0.25mol/L,故A错误;B项,同温同体积时气体压强之比等于物质的量之比,所以2s末容器内的压强与初始的压强之比为: ![]() =
=![]() ,故B正确;C项,体积分数等于物质的量分数,所以2s时C的体积分数为:
,故B正确;C项,体积分数等于物质的量分数,所以2s时C的体积分数为: ![]() =
=![]() ,故C正确;D项,2s内A反应了1mol、C生成了1mol,所以化学方程式中A与B的化学计量数应相等,即z=1,故D正确。
,故C正确;D项,2s内A反应了1mol、C生成了1mol,所以化学方程式中A与B的化学计量数应相等,即z=1,故D正确。

练习册系列答案
相关题目
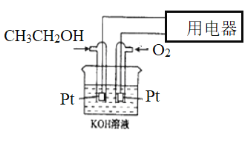
【题目】用石墨电极完成下列电解实验
实验一 | 实验二 | |
装置 |
|
|
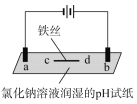
现象 | a、d处试纸变蓝;b处变红,局部褪色;c处无明显变化 | 两个石墨电极附近有气泡产生;n处有气泡产生…… |
下列对实验现象的解释或推测不合理的是( )
A. a、d处:2H2O+2e-=H2↑+2OH- B. b处:2Cl--2e-=Cl2↑
C. c处发生了反应:Fe-2e-=Fe2+ D. 根据实验一的原理,实验二中m处能析出铜