题目内容
(14分)依据题目要求回答下列问题。
(1)常温下,浓度均为0.lmol·L-1的下列六种溶液的pH如下表:
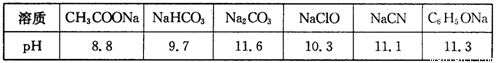
①上述盐溶液中的阴离子,结合H+能力最强的是
②根据表中数据,浓度均为0.0lmol·L-1的下列五种物质的溶液中,酸性最强的是 (填编号);将各溶液分别稀释100倍,pH变化最小的是 (填编号)
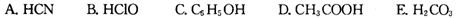
③据上表数据,请你判断下列反应不能成立的是 (填编号)
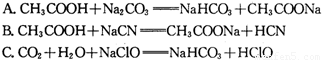
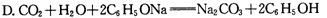
④要增大氯水中HC1O的浓度,可向氯水中加入少量的碳酸氢钠溶液,反应的离子方程式为 。
(2)已知常温下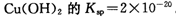 。又知常温下某CuSO4溶液里
。又知常温下某CuSO4溶液里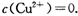
02 mol·L-1,如果要生成Cu(OH)2沉淀,则应调整溶液pH大于____.
(3)已知可逆反应 是炼铁工业中一个重要反应,其温度与平衡常数K的关系如下表:
是炼铁工业中一个重要反应,其温度与平衡常数K的关系如下表:

①写出该反应平衡常数的表达式:____ 。
②若该反应在体积固定的密闭容器中进行,在一定条件下达到平衡状态,改变下列条件:升高温度,混合气体的密度
(选填“增大”“减小”或“不变”);当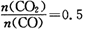 ,混合气体平均相对分子质量为
。
,混合气体平均相对分子质量为
。
(14分)(1)①CO32-(2分) ②D;C (2分) ③D(2分)
④ Cl2+HCO3-== CO2+Cl-+HClO (分步书写参照给分) (2分)
(2) 5(2分)
(3) ①c(CO2)/c(CO) (2分) ②减小,33.3(2分)
【解析】(1)考察盐类水解应用。①根据“越弱越水解”知识点,不难得出CO32-离子水解程度是最大的。②同理可以比较得到五种酸的强弱大小顺序应该是:CH3COOH > H2 CO3 > HClO > HCN > C6H5OH,稀释同样倍数条件下,酸性越小的酸变化越小。③D选项中不符合“强酸制弱酸”的原理。④氯水中生成的HCl和HClO,HCl会和HCO3-,而HClO不会和HCO3-,所有反应应该为Cl2+HCO3-== CO2+Cl-+HClO
(2)考察沉淀溶解平衡的应用。Ksp[Cu(OH)2]=c(Cu2+)·c(OH-)2,当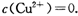 02
mol·L-1,c(OH-)=1×10-9
mol·L-1,则c(H+)
=1×10-5mol·L-1,所有PH要大于5
02
mol·L-1,c(OH-)=1×10-9
mol·L-1,则c(H+)
=1×10-5mol·L-1,所有PH要大于5
(3)考察平衡常数和平衡移动的因素。①该平衡中FeO和Fe为固体,浓度为一定值,故K= c(CO2)/c(CO);②由温度和平衡常数K关系表可知反应是放热反应,升高温度平衡逆方向移动,混合气体的密度减小;当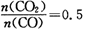 时,CO2占气体体积分数1/3,CO占气体体积分数2/3,所以混合气体平均相对分子质量为33.3
时,CO2占气体体积分数1/3,CO占气体体积分数2/3,所以混合气体平均相对分子质量为33.3

依据题目要求回答下列问题。
(1)常温下,浓度均为 0.l mol·L-1的下列六种溶液的pH如下表:
| 溶质 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN | C6H5ONa |
| pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 | 11.3 |
②浓度均为0.0l mol·L-1的下列五种物质的溶液中,酸性最强的是 (填编号);将各溶液分别稀释100倍,pH变化最小的是 (填编号)
A. HCN B. HClO C. C6H5OH D. CH3COOH E. H2CO3
③据上表数据,请你判断下列反应不能成立的是 (填编号)
A. CH3COOH + Na2CO3 = NaHCO3 + CH3COONa
B. CH3COOH + NaCN = CH3COONa + HCN
C. CO2 + H2O + NaClO = NaHCO3 + HClO
D. CO2 + H2O + 2C6H5ONa = Na2CO3 + 2C6H5OH
④要增大氯水中HC1O的浓度,可向氯水中加入少量的碳酸氢钠溶液,反应的离子方程式为 。
(2)已知常温下Cu(OH)2的Ksp=2×10—20。又知常温下某CuSO4溶液里 c(Cu2+)=0.02mol·L-1,如果要生成Cu(OH)2沉淀,则应调整溶液pH大于_ 。
依据题目要求回答下列问题。
(1)常温下,浓度均为 0.l mol·L-1的下列六种溶液的pH如下表:
|
溶质 |
CH3COONa |
NaHCO3 |
Na2CO3 |
NaClO |
NaCN |
C6H5ONa |
|
pH |
8.8 |
9.7 |
11.6 |
10.3 |
11.1 |
11.3 |
①上述盐溶液中的阴离子,结合H+能力最强的是 。
②浓度均为0.0l mol·L-1的下列五种物质的溶液中,酸性最强的是 (填编号);将各溶液分别稀释100倍,pH变化最小的是 (填编号)
A. HCN B. HClO C. C6H5OH D. CH3COOH E. H2CO3
③据上表数据,请你判断下列反应不能成立的是 (填编号)
A. CH3COOH + Na2CO3 = NaHCO3 + CH3COONa
B. CH3COOH + NaCN = CH3COONa + HCN
C. CO2 + H2O + NaClO = NaHCO3 + HClO
D. CO2 + H2O + 2C6H5ONa = Na2CO3 + 2C6H5OH
④要增大氯水中HC1O的浓度,可向氯水中加入少量的碳酸氢钠溶液,反应的离子方程式为 。
(2)已知常温下Cu(OH)2的Ksp=2×10—20。又知常温下某CuSO4溶液里 c(Cu2+)=0.02mol·L-1,如果要生成Cu(OH)2沉淀,则应调整溶液pH大于_ 。
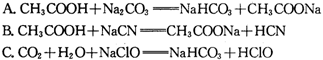
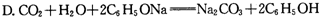
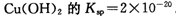 。又知常温下某CuSO4溶液里
。又知常温下某CuSO4溶液里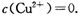
 是炼铁工业中一个重要反应,其温度与平衡常数K的关系如下表:
是炼铁工业中一个重要反应,其温度与平衡常数K的关系如下表:
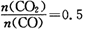 ,混合气体平均相对分子质量为 。
,混合气体平均相对分子质量为 。