题目内容
下列反应中,盐酸既作还原剂,又表现出酸的性质的是
- A.Fe+2HCl=FeCl2+H2↑
- B.CaCO3+2HCl=CaCl2+CO2↑+H2O
- C.MnO2+4HCl(浓)
 MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O - D.NaOH+HCl=NaCl+H2O
C
分析:盐酸既作还原剂,又作酸,说明该反应中部分氯化氢的化合价升高,部分氯化氢的化合价不发生变化,据此分析解答.
解答:A.该反应中,HCl中的氢离子得电子化合价降低,盐酸作氧化剂,所以与题意不相符,故A不选;
B.该反应中各元素的化合价都不发生变化,不是氧化还原反应,盐酸只作酸,所以与题意不相符,故B不选;
C.该反应中,部分氯化氢中氯元素化合价升高,部分氯化氢中的氯、氢元素的化合价都不变化,所以部分盐酸作还原剂,部分盐酸作酸,C符合题意,故C选;
D.该反应中,各元素的化合价都不发生变化,不是氧化还原反应,盐酸只作酸,所以与题意不相符,故D不选;
故选C.
点评:本题考查了氧化还原反应,明确元素化合价是解本题的关键,难度不大.
分析:盐酸既作还原剂,又作酸,说明该反应中部分氯化氢的化合价升高,部分氯化氢的化合价不发生变化,据此分析解答.
解答:A.该反应中,HCl中的氢离子得电子化合价降低,盐酸作氧化剂,所以与题意不相符,故A不选;
B.该反应中各元素的化合价都不发生变化,不是氧化还原反应,盐酸只作酸,所以与题意不相符,故B不选;
C.该反应中,部分氯化氢中氯元素化合价升高,部分氯化氢中的氯、氢元素的化合价都不变化,所以部分盐酸作还原剂,部分盐酸作酸,C符合题意,故C选;
D.该反应中,各元素的化合价都不发生变化,不是氧化还原反应,盐酸只作酸,所以与题意不相符,故D不选;
故选C.
点评:本题考查了氧化还原反应,明确元素化合价是解本题的关键,难度不大.

练习册系列答案
 黎明文化寒假作业系列答案
黎明文化寒假作业系列答案
相关题目
下列反应中,盐酸既作还原剂,又表现出酸的性质的是
A. |
B.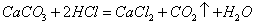 |
C.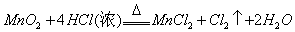 |
D. |



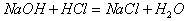
 MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O