题目内容
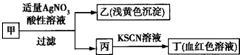
某研究小组鉴别甲的过程与现象如图所示(已知甲是一种盐).下列结论正确的是

- A.如果甲中含有S2-,则乙是硫磺沉淀
- B.如果乙是AgCl沉淀,那么甲是FeCl3
- C.丙中肯定含有Fe3+,所以甲是FeBr2
- D.甲中含有铁元素,可能显+2价或+3价
D
分析:甲与硝酸银酸性溶液反应可得乙与丙,乙为淡黄色沉淀,则乙为AgBr,丙与KSCN溶液反应呈血红色,则丙中一定含有Fe3+,但甲转化为乙和丙时的试剂书写酸性硝酸银溶液,具有强氧化性,则甲可能是溴化亚铁,也可能是溴化铁,据此解答.
解答:甲与硝酸银酸性溶液反应可得乙与丙,乙为淡黄色沉淀,则乙为AgBr,丙与KSCN溶液反应呈血红色,则丙中一定含有Fe3+,但甲转化为乙和丙时的试剂书写酸性硝酸银溶液,具有强氧化性,则甲可能是溴化亚铁,也可能是溴化铁,
A.由上述分析可知,甲中含有Fe2+或Fe3+,硫化亚铁不溶,酸性很弱,不能发生反应,S2-与Fe3+不能存在,故A错误;
B.AgCl是白色沉淀,乙不可能是AgCl,故B错误;
C.丙中一定含有Fe3+,甲转化为乙和丙时的试剂书写酸性硝酸银溶液,具有强氧化性,则甲可能是溴化亚铁,也可能是溴化铁,故C错误;
D.甲可能是溴化亚铁,也可能是溴化铁,故D正确;
故选D.
点评:本题考查离子检验,元素化合物性质等,难度中等,注意掌握常见离子检验方法,注意酸性硝酸银溶液有强氧化性.
分析:甲与硝酸银酸性溶液反应可得乙与丙,乙为淡黄色沉淀,则乙为AgBr,丙与KSCN溶液反应呈血红色,则丙中一定含有Fe3+,但甲转化为乙和丙时的试剂书写酸性硝酸银溶液,具有强氧化性,则甲可能是溴化亚铁,也可能是溴化铁,据此解答.
解答:甲与硝酸银酸性溶液反应可得乙与丙,乙为淡黄色沉淀,则乙为AgBr,丙与KSCN溶液反应呈血红色,则丙中一定含有Fe3+,但甲转化为乙和丙时的试剂书写酸性硝酸银溶液,具有强氧化性,则甲可能是溴化亚铁,也可能是溴化铁,
A.由上述分析可知,甲中含有Fe2+或Fe3+,硫化亚铁不溶,酸性很弱,不能发生反应,S2-与Fe3+不能存在,故A错误;
B.AgCl是白色沉淀,乙不可能是AgCl,故B错误;
C.丙中一定含有Fe3+,甲转化为乙和丙时的试剂书写酸性硝酸银溶液,具有强氧化性,则甲可能是溴化亚铁,也可能是溴化铁,故C错误;
D.甲可能是溴化亚铁,也可能是溴化铁,故D正确;
故选D.
点评:本题考查离子检验,元素化合物性质等,难度中等,注意掌握常见离子检验方法,注意酸性硝酸银溶液有强氧化性.

练习册系列答案
相关题目