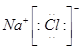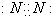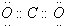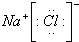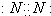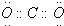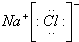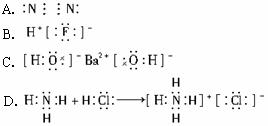题目内容
下列电子式不正确的是( )
分析:A.氯原子为成键的孤对电子对未画出;
B.氮气分子中氮原子之间形成3对共用电子对,氮原子含有1对孤对电子对;
C.二氧化碳分子中碳原子一氧原子之间形成2对共用电子对,氧原子含有2对孤对电子对;
D.氯化钠属于离子化合物,由钠离子与氯离子构成.
B.氮气分子中氮原子之间形成3对共用电子对,氮原子含有1对孤对电子对;
C.二氧化碳分子中碳原子一氧原子之间形成2对共用电子对,氧原子含有2对孤对电子对;
D.氯化钠属于离子化合物,由钠离子与氯离子构成.
解答:解:A.氯原子为成键的孤对电子对未画出,HCl分子中氢原子与氯原子之间形成1对共用电子对,电子式为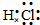 ,故A错误;
,故A错误;
B.氮气分子中氮原子之间形成3对共用电子对,氮原子含有1对孤对电子对,电子式为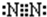 ,故B正确;
,故B正确;
C.二氧化碳分子中碳原子一氧原子之间形成2对共用电子对,氧原子含有2对孤对电子对,电子式为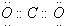 ,故C正确;
,故C正确;
D.氯化钠属于离子化合物,由钠离子与氯离子构成,电子式为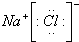 ,故D正确;
,故D正确;
故选A.
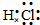 ,故A错误;
,故A错误;B.氮气分子中氮原子之间形成3对共用电子对,氮原子含有1对孤对电子对,电子式为
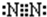 ,故B正确;
,故B正确;C.二氧化碳分子中碳原子一氧原子之间形成2对共用电子对,氧原子含有2对孤对电子对,电子式为
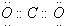 ,故C正确;
,故C正确;D.氯化钠属于离子化合物,由钠离子与氯离子构成,电子式为
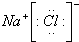 ,故D正确;
,故D正确;故选A.
点评:本题考查电子式的书写,难度中等,注意根据化学键类型与常见8电子结构书写电子式.

练习册系列答案
 永乾教育寒假作业快乐假期延边人民出版社系列答案
永乾教育寒假作业快乐假期延边人民出版社系列答案
相关题目
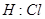 B.
B.
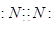 C.
C.
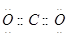 D.
D.