题目内容
(10分)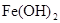 由于在空气中易被氧化,制取时很难观察到白色沉淀现象,只能看到灰绿色,采用图装置使用
由于在空气中易被氧化,制取时很难观察到白色沉淀现象,只能看到灰绿色,采用图装置使用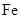 ,
,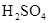 (稀),NaOH溶液可在还原性气氛中制取
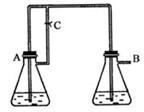
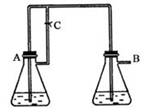
(稀),NaOH溶液可在还原性气氛中制取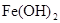 白色沉淀,且较长时间内不变色,其中C为弹簧夹,则锥形瓶A中应加入的药品为________,锥形瓶B中应加入的药品为________.容器A中的反应开始后,请设计后续操作步骤完成的制备,并说明每步操作理由和现象.
白色沉淀,且较长时间内不变色,其中C为弹簧夹,则锥形瓶A中应加入的药品为________,锥形瓶B中应加入的药品为________.容器A中的反应开始后,请设计后续操作步骤完成的制备,并说明每步操作理由和现象.

【答案】
铁和稀硫酸 氢氧化钠溶液
①打开弹簧夹C;A中气体由导管进入B,B中有气泡;目的是为了排尽装置和溶液中的氧气,形成还原性气氛;
②过一段时间,关闭弹簧夹C;A中溶液经导管进入B,B中有白色沉淀生成;因为此时A
中压强增大,使得反应生成的FeSO4溶液进入B,而和NaOH反应,生成Fe(OH)2沉淀。
【解析】要产生还原性的气体,应该用铁和稀硝酸反应生成氢气。即A中的试剂是铁和稀硫酸。利用生成的氢气排尽装置中的空气,从而可以防止氢氧化亚铁被氧化。最后利用氢气产生的越强将硫酸亚铁压入氢氧化钠中进行反应,所以B中的试剂是氢氧化钠溶液。具体的操作是①打开弹簧夹C;A中气体由导管进入B,B中有气泡;目的是为了排尽装置和溶液中的氧气,形成还原性气氛。
②过一段时间,关闭弹簧夹C;A中溶液经导管进入B,B中有白色沉淀生成;因为此时A
中压强增大,使得反应生成的FeSO4溶液进入B,而和NaOH反应,生成Fe(OH)2沉淀。

练习册系列答案
 阶梯计算系列答案
阶梯计算系列答案
相关题目
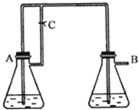 Fe(OH)2由于在空气中易被氧化,制取时很难观察到白色沉淀现象,只能看到灰绿色,采用如图装置使用Fe,H2SO4(稀),NaOH溶液可在还原性气氛中制取Fe(OH)2白色沉淀,且较长时间内不变色,其中C为弹簧夹.(提示:还原性气氛如氢气环境)
Fe(OH)2由于在空气中易被氧化,制取时很难观察到白色沉淀现象,只能看到灰绿色,采用如图装置使用Fe,H2SO4(稀),NaOH溶液可在还原性气氛中制取Fe(OH)2白色沉淀,且较长时间内不变色,其中C为弹簧夹.(提示:还原性气氛如氢气环境)