题目内容
在一个固定体积的密闭容器中,向容器中充入2mol A和1mol B,发生如下反应:2A(g)+B(g)?3C(g)+D(s),反应达到平衡时C的浓度为1.2mol/L.
(1)若使容器温度升高,平衡时混合气体中C的质量分数增加,则正反应为
(2)若维持容器体积和温度不变,按下列方法加入起始物质,达到平衡时C的浓度仍为1.2mol/L的是
①4mol A+2mol B ②3mol C+1mol D+l mol B
③3mol C+2mol D ④1.6mol A+0.8mol B+0.6mol C
(3)某温度下,向容器中加入3mol C和0.8molD,反应达到平衡时C的浓度仍为1.2mol/L,则容器的容积V应大于
(4)如果在一体积为2L的容器中充入4mol A和2mol B,维持条件和原来相同,达到平衡时C的浓度是否仍为1.2mol/L?
(1)若使容器温度升高,平衡时混合气体中C的质量分数增加,则正反应为
吸热
吸热
(填“吸热”或“放热”)反应.(2)若维持容器体积和温度不变,按下列方法加入起始物质,达到平衡时C的浓度仍为1.2mol/L的是
③
③
(用序号填空)①4mol A+2mol B ②3mol C+1mol D+l mol B
③3mol C+2mol D ④1.6mol A+0.8mol B+0.6mol C
(3)某温度下,向容器中加入3mol C和0.8molD,反应达到平衡时C的浓度仍为1.2mol/L,则容器的容积V应大于
0.5
0.5
L,小于2.5
2.5
L.(4)如果在一体积为2L的容器中充入4mol A和2mol B,维持条件和原来相同,达到平衡时C的浓度是否仍为1.2mol/L?
不一定
不一定
(填是,不是或不一定)分析:(1)容器温度升高,平衡时混合气体中C的质量分数增加,平衡向正反应移动,升高温度平衡向吸热反应移动.
(2)维持容器体积和温度不变,达到平衡时C的浓度仍为1.2mol/L,为等效平衡,且为完全等效平衡,按化学计量数转化到左边满足2mol A和1mol B.
(3)采用极限判断C的物质的量,若C未转化时,C的物质的量为3mol,此时体积最大;若D完全反应时,C平衡时的物质的量最小,此时体积最小.
(4)该反应反应前后气体的物质的量不变,体积为2L的容器中充入4mol A和2mol B,维持条件和原来相同,则反应到达平衡是与原平衡为等效平衡,各组分的含量相同,反应物的转化率相同,讨论原平衡的体积,进行判断.
(2)维持容器体积和温度不变,达到平衡时C的浓度仍为1.2mol/L,为等效平衡,且为完全等效平衡,按化学计量数转化到左边满足2mol A和1mol B.
(3)采用极限判断C的物质的量,若C未转化时,C的物质的量为3mol,此时体积最大;若D完全反应时,C平衡时的物质的量最小,此时体积最小.
(4)该反应反应前后气体的物质的量不变,体积为2L的容器中充入4mol A和2mol B,维持条件和原来相同,则反应到达平衡是与原平衡为等效平衡,各组分的含量相同,反应物的转化率相同,讨论原平衡的体积,进行判断.
解答:解:(1)根据质量守恒定律及反应方程式知,该反应反应前后气体的物质的量不变,气体的质量变小,温度升高,平衡时混合气体中C的质量分数增加,说明平衡向正反应方向移动,升高温度平衡向吸热反应移动,所以正反应是吸热反应.
故答案为:吸热.
(2)维持容器体积和温度不变,达到平衡时C的浓度仍为1.2mol/L,为等效平衡,且为完全等效平衡,按化学计量数转化到左边满足2molA和1molB即可.由2A(g)+B(g)?3C(g)+D(S)可知,
①4molA+2molB与初始A、B的物质的量不同,故①错误.
②3molC+lmolD+1molB换算成A、B,A、B物质的量分别为2mol、2mol,与初始A、B的物质的量不同,故②错误.
③3molC+2molD 换算成A、B,A、B物质的量分别为2mol、1mol,D为1mol,D是固体,对平衡无影响,故③正确.
④1.6mol A+0.8mol B+0.6molC换算成A、B,没有D,C不能反应,与初始A、B的物质的量不相同,故④错误.
故选:③.
(3)若C未转化时,C的物质的量为3mol,此时体积最大,所以容器的体积V=
=2.5L;
若D完全反应时,平衡时C的物质的量最小,此时体积最小,根据方程式计算反应的C的物质的量:
2A(g)+B(g)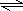 3C(g)+D(S)
3C(g)+D(S)
2.4mol 0.8mol
所以C的物质的量最小为3mol-2.4mol=0.6mol,所以容器的体积V=
=0.5L.
故答案为:0.5L;2.5L.
(4)该反应反应前后气体的物质的量不变,体积为2L的容器中充入4mol A和2mol B,维持条件和原来相同,则反应到达平衡是与原平衡为等效平衡,各组分的含量相同,反应物的转化率相同,平衡时C的物质的量是原平衡2倍.
若原平衡为1L,则该条件下到达平衡C的浓度为1.2mol/L;
若原平衡的体积不是1L,则该条件下到达平衡C的浓度不是1.2mol/L.
所以平衡时C的浓度不一定是1.2mol/L.
故答案为:不一定.
故答案为:吸热.
(2)维持容器体积和温度不变,达到平衡时C的浓度仍为1.2mol/L,为等效平衡,且为完全等效平衡,按化学计量数转化到左边满足2molA和1molB即可.由2A(g)+B(g)?3C(g)+D(S)可知,
①4molA+2molB与初始A、B的物质的量不同,故①错误.
②3molC+lmolD+1molB换算成A、B,A、B物质的量分别为2mol、2mol,与初始A、B的物质的量不同,故②错误.
③3molC+2molD 换算成A、B,A、B物质的量分别为2mol、1mol,D为1mol,D是固体,对平衡无影响,故③正确.
④1.6mol A+0.8mol B+0.6molC换算成A、B,没有D,C不能反应,与初始A、B的物质的量不相同,故④错误.
故选:③.
(3)若C未转化时,C的物质的量为3mol,此时体积最大,所以容器的体积V=
| 3mol |
| 1.2mol/L |
若D完全反应时,平衡时C的物质的量最小,此时体积最小,根据方程式计算反应的C的物质的量:
2A(g)+B(g)
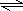 3C(g)+D(S)
3C(g)+D(S)2.4mol 0.8mol
所以C的物质的量最小为3mol-2.4mol=0.6mol,所以容器的体积V=
| 0.6mol |
| 1.2mol/L |
故答案为:0.5L;2.5L.
(4)该反应反应前后气体的物质的量不变,体积为2L的容器中充入4mol A和2mol B,维持条件和原来相同,则反应到达平衡是与原平衡为等效平衡,各组分的含量相同,反应物的转化率相同,平衡时C的物质的量是原平衡2倍.
若原平衡为1L,则该条件下到达平衡C的浓度为1.2mol/L;
若原平衡的体积不是1L,则该条件下到达平衡C的浓度不是1.2mol/L.
所以平衡时C的浓度不一定是1.2mol/L.
故答案为:不一定.
点评:本题考查的是等效平衡及化学平衡的有关计算,采用极限反应法是解(3)题的关键,采用极限反应法求出C的物质的量,从而求出容器体积范围.

练习册系列答案
相关题目