题目内容
【题目】2016杭州G20峰会期间,中美两国共同交存参加《巴黎协定》法律文书,展示了应对全球性问题的雄心和决心。其中燃煤、汽车、工业尾气排放等途径产生的CO、NOx的有效消除成为环保领域的重要课题。请根据题目提供信息回答相关问题。
Ⅰ.已知: N2(g) + O2(g) = 2NO(g) H = + 180.5 kJ·mol-1
2C(s) + O2(g) =2CO(g) H = - 221.0 kJ·mol-1
C(s) + O2(g) =CO2(g) H = - 393.5 kJ·mol-1
(1)汽车尾气转化器中发生的反应为:2NO(g) + 2CO(g) ![]() N2(g) + 2CO2(g),此反应的H =____;
N2(g) + 2CO2(g),此反应的H =____;
(2)汽车燃油不完全燃烧时产生CO,有人设想选择合适的催化剂按下列反应除去CO:2CO(g) =2C(s) + O2(g),则该反应能否自发进行并说明理由:__________________。
Ⅱ.已知:用NH3催化还原NOx时包含以下反应。
反应①:4NH3(g) + 6NO(g) ![]() 5N2(g) + 6H2O(l) H1 < 0
5N2(g) + 6H2O(l) H1 < 0
反应②:4NH3(g) + 6NO2(g) ![]() 5N2(g) + 3O2(g) + 6H2O(l) H2 > 0
5N2(g) + 3O2(g) + 6H2O(l) H2 > 0
反应③:2NO(g) + O2(g) ![]() 2NO2(g) H3 < 0
2NO2(g) H3 < 0
(3)为探究温度及不同催化剂对反应①的影响,分别在不同温度、不同催化剂下,保持其它初始条件不变重复实验,在相同时间内测得N2浓度变化情况如下图所示。下列说法正确的是__________________ 。

A.在催化剂甲的作用下反应的平衡常数比催化剂乙时大
B.反应在N点达到平衡,此后N2浓度减小的原因可能是温度升高,平衡向左移动
C.M点后N2浓度减小的原因可能是温度升高发生了副反应
D.M点后N2浓度减小的原因可能是温度升高催化剂活性降低了
(4)图中虚线为反应③在使用催化剂条件下,起始O2、NO投料比和NO平衡转化率的关系图。当其他条件完全相同时,用实线画出不使用催化剂情况下,起始O2、NO投料比和NO平衡转化率的关系示意图。__________________

(5)由NO2、O2、熔融盐NaNO3组成的燃料电池如下图所示,在使用过程中石墨Ⅰ电极反应生成一种氧化物Y,请写出石墨Ⅱ极的电极反应式:___________________ 。

【答案】 -746.5 kJ·mol-1 否,该反应△H >0,△S <0 CD  O2+4e-+ 2N2O5=4NO3-
O2+4e-+ 2N2O5=4NO3-
【解析】Ⅰ.(1)已知:①N2(g)+O2(g)═2NO(g)△H=+180.5kJ/mol,②2C(s)+O2(g)═2CO(g)△H=-221.0kJ/mol,③C(s)+O2(g)═CO2(g)△H=-393.5kJ/mol,根据盖斯定律③×2-②-①可得:2NO(g)+2CO(g)=N2(g)+2CO2(g)△H=-746.5kJ/mol,故答案为:-746.5 kJ/mol;
(2)2CO(g)=2C(s)+O2(g),该反应是焓增、熵减的反应,根据G=△H-T△S,△H>0,△S<0,△H-T△S>0,G>0,不能实现,故答案为:否,该反应△H >0,△S <0;
Ⅱ.(3)反应①为4NH3(g) + 6NO(g) ![]() 5N2(g) + 6H2O(l) H1 < 0。A.平衡常数只与温度有关,相同温度下,在催化剂甲的作用下反应的平衡常数与催化剂乙的作用下反应的平衡常数相等,故A错误;B.根据题意,用NH3催化还原NOx时包含3个反应,反应在N点达到平衡,此后N2浓度减小,原因可能是发生了副反应或催化剂活性降低,故B错误;C、D.根据题意,用NH3催化还原NOx时包含3个反应,M点后N2浓度减小,原因可能是发生了副反应或催化剂活性降低,故CD正确;故选CD;
5N2(g) + 6H2O(l) H1 < 0。A.平衡常数只与温度有关,相同温度下,在催化剂甲的作用下反应的平衡常数与催化剂乙的作用下反应的平衡常数相等,故A错误;B.根据题意,用NH3催化还原NOx时包含3个反应,反应在N点达到平衡,此后N2浓度减小,原因可能是发生了副反应或催化剂活性降低,故B错误;C、D.根据题意,用NH3催化还原NOx时包含3个反应,M点后N2浓度减小,原因可能是发生了副反应或催化剂活性降低,故CD正确;故选CD;
(4)反应③为2NO(g) + O2(g) ![]() 2NO2(g) H3 < 0。不使用催化剂情况下,反应速率减慢,到达平衡时间变长,但不影响平衡移动,平衡时CO转化率不变,不使用催化剂情况下,起始O2、NO投料比和NO平衡转化率的关系示意图为:
2NO2(g) H3 < 0。不使用催化剂情况下,反应速率减慢,到达平衡时间变长,但不影响平衡移动,平衡时CO转化率不变,不使用催化剂情况下,起始O2、NO投料比和NO平衡转化率的关系示意图为: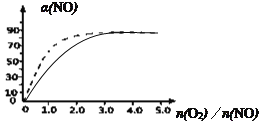 ,故答案为:
,故答案为: ;
;
(5)由图可知,石墨Ⅱ上氧气得到电子,则石墨Ⅱ为正极,石墨I上NO2失去电子,化合价升高,生成一种氧化物Y,则Y为N2O5,石墨I的电极反应为NO2+NO3--e-═N2O5,正极发生还原反应,石墨Ⅱ的电极反应式为O2+4e-+ 2N2O5=4NO3-,故答案为:O2+4e-+ 2N2O5=4NO3-。



