题目内容
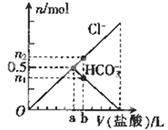
向某碳酸钠溶液中逐滴加1 mol·L─1的盐酸,测得溶液中Cl─、HCO3─的物质的量随加入盐酸体积的关系如图所示,其中n2:n1=3:2,则下列说法中正确的是 ( )

| A.Oa段反应的离子方程式与ab段反应的离子方程式相同 |
| B.该碳酸钠溶液中含有1mol Na2CO3 |
| C.b点的数值为0.6 |
| D.b点时生成CO2的物质的量为0.3 mol |
C
试题分析:注意审题,向某碳酸钠溶液中逐滴加的盐酸,考虑到应该有以下两个依次进行的反应:Na2CO3+HCl=NaCl+Na HCO3①;Na HCO3+HCl=NaCl+H2O+CO2↑②。再分析溶液中Cl─、HCO3─的物质的量随加入盐酸体积的关系图,可见Cl─的量一直在增加,而HCO3─开始和Cl─的量增加相同,到加入aml盐酸时HCO3─的量随着盐酸的加入在减少,说明这时开始发生反应②,所以A错误。加入aml盐酸时,此时溶液中Na2CO3恰好反应完,从图中可知物质的量Cl─= HCO3─=0.5mol,由反应①可知Na2CO3的物质的量应为0.5mol,所以B错误。再接着分析加入bml盐酸时,物质的量Cl─: HCO3─=3:2,由反应②可知道增加了0.1molCl─就会减少0.1mol的HCO3─,所以此时n(Cl─)=0.6mol,n(HCO3─)=0.4mol,所以此时加入盐酸的体积为0.6L,C正确。由反应②可计算反应0.1mol的HCO3─应该生成0.1mol的CO2气体,所以D错误。
其中n2:n1=3:2,
点评:熟记碳酸盐和盐酸的分步反应,再依据题意具体分析,此类属于中等难度题型。

练习册系列答案
 发散思维新课堂系列答案
发散思维新课堂系列答案
相关题目