题目内容
【题目】2019年是门捷列夫发现元素周期律150周年。下表列出了①⑧八种元素在周期表中的位置:
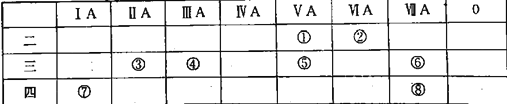
请按要求回答下列问题:
(1)写出元素②质量数为18的的核素符号_______。
(2)甲为③、⑥两元素组成的化合物,用电子式表示甲的形成过程__________。
(3)以上表中元素的最高价氧化物对应的水化物酸性最强的是_______。
(4)元素⑤的简单氢化物和元素①的简单氢化物与卤化氢的反应相似,产物的结构性质也相似。下列对元素⑤的简单氢化物与HI反应产物的推断正确的是_____(填序号)。
A.能与NaOH反应 B.含离子键、共价键 C.能与稀硫酸反应
(5)向元素⑦的单质与水反应后的溶液中加入元素④的单质,发生反应的离子反应方程式为_______。
(6)不同卤素原子之间可形成卤素互化物,其性质与卤素单质相近。写出⑥形成的互化物和SO2在水溶液中发生反应的化学方程式_______。
【答案】![]()
![]() HClO4 AB 2Al+2OH-+2H2O=2AlO2-+3H2↑ BrCl+2H2O+SO2=H2SO4+HCl+HBr
HClO4 AB 2Al+2OH-+2H2O=2AlO2-+3H2↑ BrCl+2H2O+SO2=H2SO4+HCl+HBr
【解析】
先根据元素在周期表的位置确定各种元素,然后结合元素周期律及物质的原子结构、形成化合物时的特点、元素化合物的性质分析解答。
根据元素在周期表的位置可知各种元素分别是:①是N元素,②是O元素,③是Mg元素,④是Al元素,⑤是P元素,⑥是Cl元素,⑦是K元素,⑧是Br元素。
(1)②是O元素,质子数为8,质量数为18的O原子可表示为![]() ;
;
(2)Mg、Cl两种元素形成的化合物甲为MgCl2,该物质是离子化合物,用电子式表示为:![]() ;
;
(3)元素的非金属性越强,其最高价氧化物对应的水化物的酸性越强,在上述表格中,元素最高价氧化物对应的水化物的酸性最强的是HClO4;
(4)NH3与HCl反应形成NH4Cl,由于同一主族元素形成的化合物性质相似,所以P元素的氢化物PH3与HCl反应产生的物质PH4Cl结构与NH4Cl也相似,属于离子化合物,含有离子键、极性共价键,能与强碱NaOH发生反应,产生NaCl、PH3、H2O,而不能与酸反应,故合理选项是AB;
(5)K与水反应产生KOH和氢气,向该溶液中加入Al,会发生反应产生KAlO2、H2,反应的离子方程式为:2Al+2OH-+2H2O=2AlO2-+3H2↑;
(6)不同卤素原子之间可形成卤素互化物,其性质与卤素单质相近。如⑥形成的互化物BrCl性质类似Cl2,BrCl和SO2在水溶液中发生反应,产生HCl、HBr、H2SO4,反应的化学方程式为BrCl+2H2O+SO2=H2SO4+HCl+HBr。