题目内容
【题目】I、有X、Y、Z、W四种化合物,其中X常用作焙制糕点所用的发酵粉,X、Y、Z的焰色反应均为黄色,W为无色无味的气体。这四种化合物具有下列转化关系(部分反应物、产物及反应条件已略去)。
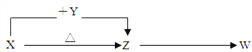
(1)W的化学式是__________;
(2)X与Y在溶液中反应的离子方程式是:___________________________;
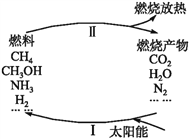
II、某混合物![]() ,含有
,含有![]() 、
、![]() 和
和![]() ,在一定条件下可实现如图所示的物质之间的变化:
,在一定条件下可实现如图所示的物质之间的变化:
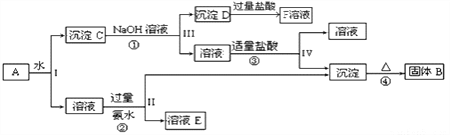
据此回答下列问题:
(1)根据上述框图反应关系,写出![]() 、
、![]() 所含物质的化学式:
所含物质的化学式:
固体![]() __________、溶液
__________、溶液![]() ______________________________
______________________________
(2)如果把步骤③中适量的盐酸改为过量的二氧化碳,则反应的离子方程式___________________________________________________________。
(3)在空气中将NaOH溶液滴入F溶液中,观察到的现象是__________________
【答案】 CO2 HCO3—+OH—=H2O+CO32— Al2O3 K2SO4、NH3·H2O、(NH4)2SO4 CO2+AlO2-+2H2O=Al(OH)3↓+HCO3- 生成红褐色沉淀
【解析】I.有X、Y、Z、W四种化合物,其中X常用作焙制糕点所用的发酵粉,X、Y、Z的焰色反应均为黄色,说明X为NaHCO3,W为无色无味的气体,再结合物质转化关系的框图可知,Z为Na2CO3、Y为NaOH、W为CO2。
(1).根据上述分析可知,W为CO2,故答案为:CO2;
(2). NaHCO3与NaOH在溶液中反应的离子方程式为:HCO3—+OH—=H2O+CO32—,故答案为:HCO3—+OH—=H2O+CO32—。
II.KAl(SO4)2可溶于水,Al2O3和Fe2O3不溶于水,混合物A加水溶解后,经过滤分离得KAl(SO4)2溶液,沉淀C含Al2O3和Fe2O3,C中加入NaOH溶液,NaOH和Al2O3反应生成NaAlO2,过滤后得到NaAlO2溶液,沉淀D为Fe2O3,加入盐酸得到溶液F为FeCl3,NaAlO2溶液中加入适量盐酸,反应生成Al(OH)3和NaCl,Al(OH)3加热分解生成B为Al2O3,KAl(SO4)2与过量氨水反应得到溶液E为K2SO4和(NH4)2SO4混合物,且含过量氨水。
(1).根据上述分析可知,固体B为Al2O3,溶液E中含有K2SO4和(NH4)2SO4、NH3·H2O,故答案为:Al2O3;K2SO4、NH3·H2O、(NH4)2SO4;
(2).向NaAlO2溶液中通入过量的二氧化碳,反应生成和Al(OH)3沉淀和NaHCO3,该反应的离子方程式为:CO2+AlO2—+2H2O=Al(OH)3↓+HCO3—,故答案为:CO2+AlO2—+2H2O=Al(OH)3↓+HCO3—;
(3).F为FeCl3溶液,将NaOH溶液滴入F溶液中,将会生成Fe(OH)3红褐色沉淀,故答案为:生成红褐色沉淀。