题目内容
下列微粒中,其核外电子数相同


| A.①②③ | B.②③④ | C.①②④ | D.①③④ |
C
试题分析:铝离子(
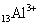 )、氟离子(
)、氟离子(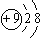 、
、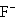 )的核外电子数均为10个,而氯离子(
)的核外电子数均为10个,而氯离子(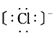 )的核外电子数为18个。
)的核外电子数为18个。
练习册系列答案
 鹰派教辅衔接教材河北教育出版社系列答案
鹰派教辅衔接教材河北教育出版社系列答案 初中暑期衔接系列答案
初中暑期衔接系列答案
相关题目
题目内容

| A.①②③ | B.②③④ | C.①②④ | D.①③④ |
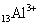 )、氟离子(
)、氟离子(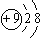 、
、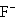 )的核外电子数均为10个,而氯离子(
)的核外电子数均为10个,而氯离子(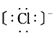 )的核外电子数为18个。
)的核外电子数为18个。
 鹰派教辅衔接教材河北教育出版社系列答案
鹰派教辅衔接教材河北教育出版社系列答案 初中暑期衔接系列答案
初中暑期衔接系列答案