题目内容
18.取相同质量的甲烷和有机物A、B,跟氧气分别完全燃烧后,生成的二氧化碳的物质的量都相同.有机物A是饱和一元醇,有机物B是饱和一元醛.(1)写出分子式:AC9H20O,BC8H16O.
(2)若符合题给的燃烧产物与反应物的关系,A、B有机物必须满足的条件是含碳的质量分数与甲烷的相同.
分析 (1)根据A是饱和一元醇、B是饱和一元醛设出A、B的分子式,然后利用A、B分子中含碳量与甲烷的相同列式确定二者的分子式;
(2)质量相同时设出的二氧化碳的物质的量相同,说明有机物分子中含有的碳元素的质量分数相同.
解答 解:(1)相同质量的甲烷和有机物A、B,跟氧气分别完全燃烧后,生成的二氧化碳的物质的量都相同,说明A、B含碳的质量分数与甲烷的相同,
又知A是饱和一元醇,其分子式符合CnH2n+2O,则:$\frac{12}{16}$=$\frac{12n}{14n+2+16}$,解得:n=9,故A的分子式为C9H20O;
有机物B是饱和一元醛,其分子式符合CnH2nO,则:$\frac{12}{16}$=$\frac{12n}{14n+16}$,解得:n=8,故A的分子式为C8H16O,
故答案为:C9H20O; C8H16O;
(2)质量相同时A、B完全燃烧生成的二氧化碳与等质量的甲烷完全燃烧生成的二氧化碳的物质的量相等,说明有机物A、B分子中含碳的质量分数与甲烷的相同,
故答案为:含碳的质量分数与甲烷的相同.
点评 本题考查了有机物分子式确定的计算,题目难度中等,明确常见有机物结构与性质为解答关键,试题侧重考查学生的分析能力及化学计算能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
8.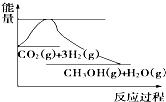 实现“节能减排”和“低碳经济”的一项重要课题就是如何将CO2转化为可利用的资源.目前工业方法是用CO2来生产燃料甲醇.一定条件下发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g),下图表示该反应过程中能量(单位为kJ•mol-1)的变化:关于该反应的下列说法中,正确的是( )
实现“节能减排”和“低碳经济”的一项重要课题就是如何将CO2转化为可利用的资源.目前工业方法是用CO2来生产燃料甲醇.一定条件下发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g),下图表示该反应过程中能量(单位为kJ•mol-1)的变化:关于该反应的下列说法中,正确的是( )
 实现“节能减排”和“低碳经济”的一项重要课题就是如何将CO2转化为可利用的资源.目前工业方法是用CO2来生产燃料甲醇.一定条件下发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g),下图表示该反应过程中能量(单位为kJ•mol-1)的变化:关于该反应的下列说法中,正确的是( )
实现“节能减排”和“低碳经济”的一项重要课题就是如何将CO2转化为可利用的资源.目前工业方法是用CO2来生产燃料甲醇.一定条件下发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g),下图表示该反应过程中能量(单位为kJ•mol-1)的变化:关于该反应的下列说法中,正确的是( )| A. | △H<0,△S<0 | B. | △H>0,△S<0 | C. | △H>0,△S>0 | D. | △H<0,△S>0 |
9.下列说法正确的是( )
①江河入海口三角洲的形成通常与胶体的性质有关
②“钡餐”中使用的硫酸钡是弱电解质
③冰和干冰既是纯净物又是化合物
④雾是气溶胶,在阳光下可观察到丁达尔现象
⑤某无色溶液中加入稀盐酸,产生的气体可使澄清石灰水变浑浊,则原溶液中一定含CO${\;}_{3}^{2-}$
⑥可用渗析法分离Fe(OH)3胶体和KCl溶液.
①江河入海口三角洲的形成通常与胶体的性质有关
②“钡餐”中使用的硫酸钡是弱电解质
③冰和干冰既是纯净物又是化合物
④雾是气溶胶,在阳光下可观察到丁达尔现象
⑤某无色溶液中加入稀盐酸,产生的气体可使澄清石灰水变浑浊,则原溶液中一定含CO${\;}_{3}^{2-}$
⑥可用渗析法分离Fe(OH)3胶体和KCl溶液.
| A. | ①③④⑤ | B. | ①③④⑥ | C. | ①③④⑤⑥ | D. | ①②③④⑤⑥ |
13.为了测定酸碱反应的反应热,计算时至少需要的数据是( )
①酸的浓度和体积 ②碱的浓度和体积 ③比热容 ④反应后溶液的质量
⑤反应前后溶液温度变化 ⑥操作所需的时间.
①酸的浓度和体积 ②碱的浓度和体积 ③比热容 ④反应后溶液的质量
⑤反应前后溶液温度变化 ⑥操作所需的时间.
| A. | ①②③⑤ | B. | ①③④⑥ | C. | ③④⑤⑥ | D. | 全部 |
3.在指定环境中可能大量共存的离子组是( )
| A. | 在c(H+)=1.0×10-13mol•L-1的溶液中:Na+、S2-、AlO2-、SO32- | |
| B. | 在由水电离出的c(H+)=1×10-12mol/L的溶液中:Fe2+ NO3- Na+ SO42- | |
| C. | 使甲基橙变红的溶液中:NH4+、K+、ClO-、Cl- | |
| D. | 能与Al反应放出H2的溶液中:K+、Cu2+、Cl-、NO3- |
10.下列关于二氧化硫的说法正确的是( )
| A. | 二氧化硫是无色无味无毒的气体 | B. | 二氧化硫不是形成酸雨的主要成分 | ||
| C. | 二氧化硫可以与水反应形成硫酸 | D. | 二氧化硫可以使品红褪色 |
7.硅元素有质量数为28、29、30三种同位素,硅元素的近似相对原子质量为28.1,自然界中质量数为28的硅原子百分含量为92%,则质量分数为29、30的原子个数比为( )
| A. | 3:5 | B. | 3:1 | C. | 2:3 | D. | 3:2 |
7.下列各组物质相互反应,能产生可燃性气体的是( )
| A. | 电石投入食盐水 | B. | 铜投入浓硝酸 | ||
| C. | 炭投入热的浓硫酸 | D. | 碳酸钙投入盐酸 |
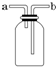 如图所示装置是化学实验室中的常用装置,它有多种用途,以下各项用途和操作都正确的是C(填序号).
如图所示装置是化学实验室中的常用装置,它有多种用途,以下各项用途和操作都正确的是C(填序号).