题目内容
下列反应中,属于氧化还原反应的是( )
A.SO2+2KOH=K2SO3+H2O
B.CaCO3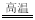 CaO+CO2↑
CaO+CO2↑
C.Na2CO3+CaCl2=CaCO3↓+2NaCl
D.Fe+2FeCl3=3FeCl2
D
【解析】
试题分析:A、B、C三个化学反应均无化合价的变化,故不属于氧化还原反应。D、反应中铁中的化合价发生了变化,故是氧化还原反应。
考点:氧化还原反应的判断

 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案现有下列十种物质:
①H2;②铝;③CaO;④CO2;⑤H2SO4;⑥Ba(OH)2;⑦红褐色的氢氧化铁液体;⑧氨水;⑨稀硝酸;⑩Al2(SO4)3
上述各物质按物质的分类方法填写表格的空白处(填物质编号):
分类标准 | 金属单质 | 氧化物 | 溶液 | 胶体 | 电解质 |
属于该类的物质 |
|
|
|
|
|
(2)上述十种物质中有两种物质之间可发生离子反应:H++OH-= H2O,该离子反应对应的化学方程式为 。
(3)⑩在水中的电离方程式为 ,
(4)少量的④通入⑥的溶液中反应的离子方程式为 。
(5)②与⑨发生反应的化学方程式为:Al + 4HNO3 = Al(NO3)3 + NO↑ + 2H2O,该反应的氧化剂是 (填化学式),氧化剂与还原剂的物质的量之比是 ,当有5.4g Al发生反应时,转移电子的物质的量为 。该反应的离子方程式为 。