题目内容
【题目】对于密闭容器中可逆反应 A2(g)+3B2(g)![]() 2AB3(g),探究单一条件改变情况下,可能引起平衡状态的改变,得到如下图所示的曲线(图中T表示温度,n 表示物质的量)下列判断正确的是( )
2AB3(g),探究单一条件改变情况下,可能引起平衡状态的改变,得到如下图所示的曲线(图中T表示温度,n 表示物质的量)下列判断正确的是( )

A.加入催化剂可以使状态 d 变为状态 b
B.若 T1>T2,则逆反应一定是放热反应
C.达到平衡时 A2 的转化率大小为: b>a>c
D.在T2 和n(A2)不变时达到平衡,AB3 的物质的量大小为: c>b>a
【答案】D
【解析】
试题分析:A.催化剂只改变反应速率不改变平衡移动,所以加入催化剂不可能使状态d变为状态b,故A错误;B.若T1>T2,由图象可知温度升高AB3的平衡体积分数减小,说明升高温度平衡向逆反应分析移动,则逆反应为吸热反应,故B错误;C.由图可知,横坐标为B2的物质的量,增大一种反应物的量会促进另一种反应物的转化率增大,则B2越大达到平衡时A2的转化率越大,即达到平衡时A2的转化率大小为c>b>a,故C错误;D.由图可知,横坐标为B2的物质的量,增大一种反应物的量必然会促进另一种反应物的转化,则B2越大达到平衡时A2的转化率越大,生成物的物质的量越大,则平衡时AB3的物质的量大小为:c>b>a,故D正确;故选D。

练习册系列答案
 全优考典单元检测卷及归类总复习系列答案
全优考典单元检测卷及归类总复习系列答案 品学双优卷系列答案
品学双优卷系列答案 小学期末冲刺100分系列答案
小学期末冲刺100分系列答案
相关题目
【题目】用如图所示装置进行下列实验:将①中溶液滴入②中,预测的现象与实际相符的是
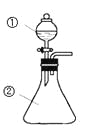
选项 | ①中物质 | ②中物质 | 预测②中的现象 |
A | 稀盐酸 | 碳酸钠与氢氧化钠的混合溶液 | 立即产生气泡 |
B | 浓硝酸 | 用砂纸打磨过的铝条 | 产生红棕色气体 |
C | 氯化铝溶液 | 浓氢氧化钠溶液 | 产生大量白色沉淀 |
D | 草酸溶液 | 酸性高锰酸钾溶液 | 溶液逐渐褪色 |
A. A B. B C. C D. D