题目内容
已知A、B两种元素是位于元素周期表中同一周期的两种元素,它们的最高价氧化物的水化物的分子式分别为H3AO4和H2BO4,且分子量相同;A的气态氢化物含氢量8.82%,并且A、B两元素的原子中含有的中子数相等.试回答:(1)通过计算确定A、B两元素的名称;
(2)比较H3AO4和H2BO4的酸性强弱.
答案:
解析:
解析:
| 解析:问题(1)是解题的关键,而解问题(1)的途径在于分析A、B两元素最高价氧化物的水化物分子式与它们在元素周期表中的位置关系.由元素周期表与各元素一般化合物的通式的关系,可知A元素处于第ⅤA族,B元素处于第ⅥA族,进而又可推知A的氢化物的通式为AH3,然后利用其含氢百分率即可计算出A的相对原子质量为31,A为磷元素,最后利用H3AO4和H2BO4的分子量相同,且A、B原子的中子数相同,不难推出B为硫元素.问题(2)是元素周期表和元素周期律的具体应用,我们只须分析硫和磷在元素周期表中的相对位置,然后利用元素周期律的知识即可得出结论.
答案:(1)A为磷、B为硫 (2)酸性H2SO4大于磷酸.
|

练习册系列答案
相关题目
| |||||||||||||||||||||||
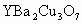 .求:
.求: .求:
.求: