题目内容
14.下列鉴别方法不可行的是( )| A. | 只用溴水一种试剂不能鉴别苯、己烯、乙醇、四氯化碳 | |
| B. | 用新制氢氧化铜悬浊液鉴别甲酸甲酯和乙酸两种液体 | |
| C. | 不能用李比希法,可用核磁共振氢谱法鉴别1-溴丙烷和2-溴丙烷 | |
| D. | 检验卤代烃中的卤原子种类:先向卤代烃中滴加氢氧化钠醇溶液并加热,冷却后滴加足量稀硝酸酸化,最后滴加硝酸银溶液,观察沉淀颜色,进而确定卤原子种类 |
分析 A、苯、己烯、乙醇、四氯化碳分别与溴水混合的现象为:分层后有机层在上层、溴水褪色、不分层、分层后有机层在下层;
B、乙酸、甲酸甲酯分别与氢氧化铜悬浊液混合,现象分别为蓝色溶液、砖红色沉淀;
C、根据l-溴丙烷和2-溴丙烷的中有几种不同的H原子分析;
D、检验溴乙烷中溴元素,应在碱性条件下水解,最后加入硝酸酸化,加入硝酸银.
解答 解:A、苯、己烯、乙醇、四氯化碳分别与溴水混合的现象为:分层后有机层在上层、溴水褪色、不分层、分层后有机层在下层,现象不同,可鉴别,故A错误;
B、乙酸是一种酸,能将氢氧化铜悬浊液溶解,得蓝色溶液;甲酸甲酯中含醛基,和新制氢氧化铜悬浊液反应生成砖红色沉淀,现象不同故可鉴别,故B正确;
C、l-溴丙烷的结构简式为CH2BrCH2CH3,含有3种不同的H原子,2-溴丙烷的结构简式为CH3CHBrCH3,含有2种不同的H原子,用核磁共振氢谱可以鉴别l-溴丙烷和2-溴丙烷,故C正确;
D、检验卤代烃中的卤原子:加入NaOH醇溶液共热,卤代烃消去生成卤离子,然后加入稀硝酸至溶液呈酸性,再加AgNO3溶液,观察沉淀的颜色,故D正确.
故选A.
点评 本题考查了有机物的鉴别和官能团的检验,应注意的是乙酸能和新制的氢氧化铜溶液发生酸碱中和,使氢氧化铜悬浊液溶解.

练习册系列答案
相关题目
5.重水(D2O)是重要的核工业原料,下列说法错误的是( )
| A. | 氘(D)原子核外有1个电子 | |
| B. | 1H218O与D216O的相对分子质量相同 | |
| C. | H2O与D2O互称同素异形体 | |
| D. | 1H与D互称同位素 |
2.在2A(g)+B(g)=3C(g)+4D(g)反应中,表示该反应速率最快的是( )
| A. | υ(A)=0.5 mol•(L•s)-1 | B. | υ(B)=0.3 mol•(L•s)-1 | ||
| C. | υ(C)=0.8 mol•(L•s)-1 | D. | υ(D)=1 mol•(L•s)-1 |
9.下列各选项陈述Ⅰ和陈述Ⅱ均正确且二者有因果关系的是( )
| 陈述Ⅰ | 陈述Ⅱ | |
| A | NaHCO3为强碱弱酸盐,只存在水解平衡 | NaHCO3溶液显碱性 |
| B | HCL与Na2CO3溶液反应生成CO2 | 用饱和NaCO3溶液除去CO2中的少量HCl |
| C | Cl2使润湿的有色布条褪色,而干燥的布条不褪色 | 次氯酸的氧化性比氯气的强 |
| D | 常温下铁、铜均不溶于浓硫酸 | 常温下铁、铜与浓硫酸均不反应 |
| A. | A | B. | B | C. | C | D. | D |
19.日常所用锌-锰干电池的电极分别为锌筒和石墨棒,以糊状NH4Cl作电解质,电极反应为:Zn-2e-=Zn2+,2MnO2+2NH4++2e-=Mn2O3+2NH3+H2O.下列有关锌-锰干电池的叙述中,正确的是( )
| A. | 干电池中锌筒为正极,石墨棒为负极 | |
| B. | 干电池长时间连续工作后,糊状物可能流出,腐蚀用电器 | |
| C. | 干电池工作时,电流方向是由锌筒经外电路流向石墨棒 | |
| D. | 干电池可实现化学能向电能和电能向化学能的相互转化 |
6.下列溶液中NO3-的物质的量最大的是( )
| A. | 500mL1mol/L的KNO3溶液 | B. | 500mL1mol/L的Ba(NO3)2溶液 | ||
| C. | 100mL0.5mol/L的Mg(NO3)2溶液 | D. | 1L0.5mol/L的Fe(NO3)3溶液 |
3.气体甲能使湿润的红色石蕊试纸变蓝,气体乙可在空气中产生白雾,当甲与乙相遇时可能生成( )
| A. | NH4C1 | B. | NH4HCO3 | C. | (NH4)2CO3 | D. | (NH4)2SO4 |
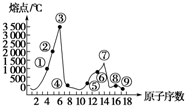 如图是部分短周期元素的单质熔点的变化图,根据此图,填写下列空格:
如图是部分短周期元素的单质熔点的变化图,根据此图,填写下列空格: .
.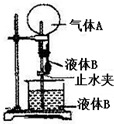 如图是实验室进行“喷泉”实验的一种装置,使用下列物质一定不会出现“喷泉”现象的是( )
如图是实验室进行“喷泉”实验的一种装置,使用下列物质一定不会出现“喷泉”现象的是( )