题目内容
在一定条件下,反应N2 + 3H2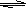 2NH3,在2L密闭容器中进行,5min内氨的质量增加了1.7 g,则反应速率为
2NH3,在2L密闭容器中进行,5min内氨的质量增加了1.7 g,则反应速率为
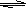 2NH3,在2L密闭容器中进行,5min内氨的质量增加了1.7 g,则反应速率为
2NH3,在2L密闭容器中进行,5min内氨的质量增加了1.7 g,则反应速率为| A.v(H2)="0.03" mol/(L·min) | B.v(N2)="0.02" mol/(L·min) |
| C.v(NH3)="0.01" mol/(L·min) | D.v(NH3)="0.17" mol/(L·min) |
C
试题分析:1.7g氨气的物质的量是1.7g÷17/mol=0.1mol,则氨气的浓度是0.1mol÷2L=0.05mol/L,所以氨气的反应速率是0.05mol/L÷5min=0.01 mol/(L·min),选项C正确,D不正确;又因为反应速率之比是相应的化学计量数之比,则氢气和氮气反应速率分别是0.015 mol/(L·min)和0.005 mol/(L·min),选项AB不正确,答案选C。
点评:该题是基础性试题的考查,也是高考中的常见考点,难度不大。该题的关键是明确反应速率的含义和计算依据,特别是反应速率与化学计量数的关系,有利于培养学生的逻辑推理能力,有助于提高学生的学习效率。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
 2AB3(g)反应来说,下列所表示的化学反应速率中最大的是
2AB3(g)反应来说,下列所表示的化学反应速率中最大的是

 ,5min内氨的质量增加了1.7g,则反应速率为( )
,5min内氨的质量增加了1.7g,则反应速率为( )



 3C+4D在下列四种状态下不处于平衡状态的是( )
3C+4D在下列四种状态下不处于平衡状态的是( ) B(g) +C(g)在容积为1.0L的密闭容器中进行,A的初始浓度为0.050mol/L。温度T1和T2下A的浓度与时间关系如图所示。回答下列问题:
B(g) +C(g)在容积为1.0L的密闭容器中进行,A的初始浓度为0.050mol/L。温度T1和T2下A的浓度与时间关系如图所示。回答下列问题:
 nZ(g)+2W(g)。5 min末生成0.2 mol W,若测知以Z浓度变化表示的平均反应速率为0.01 mol·(L·min)-1,则n的值为( )
nZ(g)+2W(g)。5 min末生成0.2 mol W,若测知以Z浓度变化表示的平均反应速率为0.01 mol·(L·min)-1,则n的值为( )