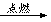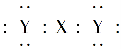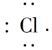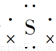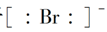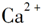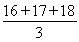题目内容
已知某物质主要成分的化学式为XY2,X原子的结构示意图为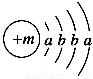 ,X的阳离子与Y的阴离子的电子层结构相同。元素Z、W均为短周期元素,它们原子的最外层电子数均是其电子层数的2倍,Z与Y相邻且Z、W能形成一种WZ2型分子。
,X的阳离子与Y的阴离子的电子层结构相同。元素Z、W均为短周期元素,它们原子的最外层电子数均是其电子层数的2倍,Z与Y相邻且Z、W能形成一种WZ2型分子。
(1)m=________,该物质主要成分的化学式为________。
(2)Z、W元素的名称为________、________。
(3)下列说法正确的是________。
A.XY2和WZ2都为离子化合物
B.XY2分子中仅含离子键,WZ2中仅含极性共价键
C.H2Z比HY的稳定性强
D.X的阳离子比Y的阴离子半径大
(4)下列化学用语表达正确的是________。

(5)水的沸点比H2Z的沸点高,其原因是_________________________________________。
(1)20 CaCl2
(2)硫 碳
(3)B
(4)BD
(5)水分子中含有氢键
【解析】(1)由X原子的结构示意图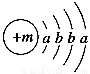 不难推知其为
不难推知其为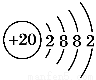 ,该元素为Ca,根据CaY2可知Y为-1价,又因Y-与Ca2+的电子层结构相同,可知Y为Cl。(2)Z、W原子的最外层电子数是其电子层数的2倍,则Z、W是C或S。Z与Y相邻,则Z是S,W是C。(3)CaCl2是仅含离子键的离子化合物,CS2是仅含极性键的共价化合物,A项错,B项对;S的非金属性弱于Cl,则H2S的稳定性比HCl弱,C项错;Ca2+、Cl-具有相同的电子层结构,但Ca元素的核电荷数大,半径小,D项错。(4)XY2为CaCl2,其电子式为
,该元素为Ca,根据CaY2可知Y为-1价,又因Y-与Ca2+的电子层结构相同,可知Y为Cl。(2)Z、W原子的最外层电子数是其电子层数的2倍,则Z、W是C或S。Z与Y相邻,则Z是S,W是C。(3)CaCl2是仅含离子键的离子化合物,CS2是仅含极性键的共价化合物,A项错,B项对;S的非金属性弱于Cl,则H2S的稳定性比HCl弱,C项错;Ca2+、Cl-具有相同的电子层结构,但Ca元素的核电荷数大,半径小,D项错。(4)XY2为CaCl2,其电子式为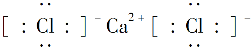 ;H2S的水溶液为弱酸,应写成分子式,即Cl2+H2S=2H++2Cl-+S↓,A、C两项错。(5)氢键影响物质的熔、沸点,使水的沸点升高。
;H2S的水溶液为弱酸,应写成分子式,即Cl2+H2S=2H++2Cl-+S↓,A、C两项错。(5)氢键影响物质的熔、沸点,使水的沸点升高。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目