题目内容
为了证明乙醇分子中含有氧原子,现采用一套装置进行实验,试根据下列装置中的试剂及实验现象,回答有关问题:
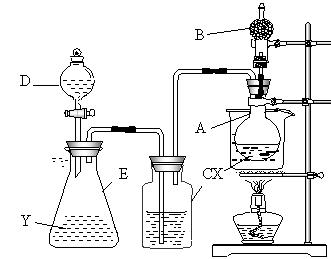
(1)装置中所装的试剂:①A瓶装无水乙醇,内放无水盐X;
②B干燥管里装生石灰;
③C和D中都装浓H2SO4;
④E瓶装试剂Y;
(2)实验现象及操作:用水浴加热A瓶:将D中浓H2SO4缓缓滴入E中与试剂Y作用,发现C中导管有大量气泡放出;A瓶内X逐渐变色,从B中挥发出的气体可点燃。
回答下列问题:
(1)E瓶里所装的试剂Y是____________。
①饱和食盐水 ②MnO2和NaCl的混合物 ③浓HCl
(2)D中浓H2SO4所起的作用是_________________,C中浓H2SO4所起的作用是__________。
(3)A瓶中发生反应的化学方程式是____________________;反应类型是___________;所生成的_________(写名称)在B出口处点燃。
(4)无水盐X宜选用__________;它能起指示剂作用的原因是____________________。
(5)此实验能证明乙醇分子中含有氧原子的理由是____________________。
(6)如果将装置中的C瓶去掉能否得出最终结论?____________________。为什么?

(1)装置中所装的试剂:①A瓶装无水乙醇,内放无水盐X;
②B干燥管里装生石灰;
③C和D中都装浓H2SO4;
④E瓶装试剂Y;
(2)实验现象及操作:用水浴加热A瓶:将D中浓H2SO4缓缓滴入E中与试剂Y作用,发现C中导管有大量气泡放出;A瓶内X逐渐变色,从B中挥发出的气体可点燃。
回答下列问题:
(1)E瓶里所装的试剂Y是____________。
①饱和食盐水 ②MnO2和NaCl的混合物 ③浓HCl
(2)D中浓H2SO4所起的作用是_________________,C中浓H2SO4所起的作用是__________。
(3)A瓶中发生反应的化学方程式是____________________;反应类型是___________;所生成的_________(写名称)在B出口处点燃。
(4)无水盐X宜选用__________;它能起指示剂作用的原因是____________________。
(5)此实验能证明乙醇分子中含有氧原子的理由是____________________。
(6)如果将装置中的C瓶去掉能否得出最终结论?____________________。为什么?
(1)③(2)吸收浓HCl中的水分,使HCl气体逸出;干燥HCl气体(3)CH3CH2OH+HCl CH3CH2Cl+H2O;取代反应;氯乙烷(4)无水CuSO4;实验过程中观察到无水CuSO4变蓝,证明反应有水生成(5)无水CuSO4变蓝证明有水生成,水中含氧元素,它不可能来自HCl,只能来自乙醇(6)不能;若不除去水,无法判断使无水CuSO4变蓝的水是否来自于乙醇与HCl的反应。
CH3CH2Cl+H2O;取代反应;氯乙烷(4)无水CuSO4;实验过程中观察到无水CuSO4变蓝,证明反应有水生成(5)无水CuSO4变蓝证明有水生成,水中含氧元素,它不可能来自HCl,只能来自乙醇(6)不能;若不除去水,无法判断使无水CuSO4变蓝的水是否来自于乙醇与HCl的反应。
 CH3CH2Cl+H2O;取代反应;氯乙烷(4)无水CuSO4;实验过程中观察到无水CuSO4变蓝,证明反应有水生成(5)无水CuSO4变蓝证明有水生成,水中含氧元素,它不可能来自HCl,只能来自乙醇(6)不能;若不除去水,无法判断使无水CuSO4变蓝的水是否来自于乙醇与HCl的反应。
CH3CH2Cl+H2O;取代反应;氯乙烷(4)无水CuSO4;实验过程中观察到无水CuSO4变蓝,证明反应有水生成(5)无水CuSO4变蓝证明有水生成,水中含氧元素,它不可能来自HCl,只能来自乙醇(6)不能;若不除去水,无法判断使无水CuSO4变蓝的水是否来自于乙醇与HCl的反应。略

练习册系列答案
 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案
相关题目

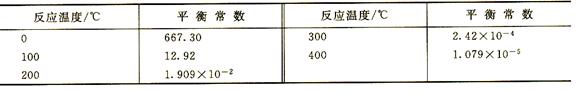
 CH3OH的平衡常数,工业上采用稍高的压强(5MPa)和250℃,其可能原因是: ▲ 。
CH3OH的平衡常数,工业上采用稍高的压强(5MPa)和250℃,其可能原因是: ▲ 。