题目内容
A是一种无色透明的晶体,进行如下实验。
①取少量A晶体做焰色反应实验,透过蓝色钴玻璃观察,火焰呈紫色。
②取少量A晶体溶于水可以得到无色的溶液,该溶液使石蕊变红。
③取少量A的溶液加过量氨水,有白色沉淀B生成。
④过滤除去③中的B后,在滤液中滴加氯化钡溶液,有白色沉淀C生成,C不溶于稀硝酸。
⑤取少量B滴加氢氧化钠溶液,得无色溶液D。
⑥取少量B滴加盐酸,得无色溶液E。
⑦将47.4 g A晶体在120℃下加热脱水,剩余物的质量为25.8 g。
根据上述实验和结果确定A、B、C、D、E,写出它们的化学式。
A________;B________;C________;D________;E________。
KAl(SO4)2·12H2O Al(OH)3 BaSO4 NaAlO2 AlCl3
【解析】由实验①知晶体含钾元素,由实验④知晶体中含有SO42-,由实验②③⑤⑥知B是Al(OH)3,晶体A中含有Al3+,故综合①~⑥知A是KAl(SO4)2·xH2O,由⑦所给数据可求出x=12,由此可确定A及其他物质的化学式。

几种短周期元素的原子半径及主要化合价如下表:
| 元素代号 | X | Y | Z | M | R |
| 原子半径/nm | 0.186 | 0.102 | 0.075 | 0.074 | 0.143 |
| 主要化合价 | +1 | +6 -2 | +5 -3 | -2 | +3 |
已知X是短周期中最活泼的金属,且与R同周期。下列叙述不正确的是 ( )
A.离子半径大小:R3+<X+< M2-
B.Y与M组成的化合物是光化学烟雾的原因之一
C.将YM2通入Ba(NO3)2溶液中有大量白色沉淀产生
D.M氢化物的熔沸点高于Z氢化物的熔沸点
下列物质分类的正确组合是( )
| 碱 | 酸 | 盐 | 酸性氧化物 | |
| A | 纯碱 | HNO3 | NaHCO3 | SO2 |
| B | 烧碱 | H2SO4 | NaCl | CO |
| C | 苛性钠 | CH3COOH | 石灰石 | 水 |
| D | 熟石灰 | H2CO3 | 纯碱 | SO3 |
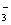 、SO
、SO 、 B.Na+、Ba2+、CO
、 B.Na+、Ba2+、CO 、NO
、NO