��Ŀ����
����������Ϣ��ҵ����Ҫ�Ļ������ϡ�ͨ����̼�ڸ����»�ԭ���������Ƶôֹ裨�����������������ʣ����ֹ���������Ӧ�������Ȼ��裨��Ӧ�¶�450-500��C�������Ȼ��辭�ᴿ����������ԭ�ɵøߴ��衣������ʵ�����Ʊ����Ȼ����װ��ʾ��ͼ��
![]()

![]() �����Ϣ���£�
�����Ϣ���£�![]()
![]()
![]()
![]()
![]()
![]()
![]()
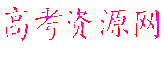
![]() a.���Ȼ�����ˮ����ˮ�⣻
a.���Ȼ�����ˮ����ˮ�⣻
![]() b.�������������ڸ����¾���������ֱ�ӷ�Ӧ������Ӧ���Ȼ��
b.�������������ڸ����¾���������ֱ�ӷ�Ӧ������Ӧ���Ȼ��
![]() c.�й����ʵ������������±���
c.�й����ʵ������������±���
![]()

![]() ��ش��������⣺
��ش��������⣺
![]() ��1��д��װ��A�з�����Ӧ�����ӷ���ʽ ��
��1��д��װ��A�з�����Ӧ�����ӷ���ʽ ��
![]() ��2��װ��A��g�ܵ������� ��װ��C�е��Լ��� ��װ��E�е�hƿ��Ҫ��ȴ������ ��
��2��װ��A��g�ܵ������� ��װ��C�е��Լ��� ��װ��E�е�hƿ��Ҫ��ȴ������ ��
![]() ��3��װ��E��hƿ�ռ����Ĵֲ����ͨ���������ƶ�����õ��ߴ������Ȼ��裬�����IJ������У�����Ԫ������ܻ����е�����Ԫ���� ����дԪ�ط��ţ���
��3��װ��E��hƿ�ռ����Ĵֲ����ͨ���������ƶ�����õ��ߴ������Ȼ��裬�����IJ������У�����Ԫ������ܻ����е�����Ԫ���� ����дԪ�ط��ţ���
![]() ��4��Ϊ�˷�������������Ԫ�صĺ������Ƚ�������Ԥ����������Ԫ�ػ�ԭ��Fe2+ ������KMnO4����Һ�����������½���������ԭ�ζ�����Ӧ�����ӷ���ʽ�ǣ�
��4��Ϊ�˷�������������Ԫ�صĺ������Ƚ�������Ԥ����������Ԫ�ػ�ԭ��Fe2+ ������KMnO4����Һ�����������½���������ԭ�ζ�����Ӧ�����ӷ���ʽ�ǣ�
![]()
![]()
![]() �ٵζ�ǰ�Ƿ�Ҫ�μ�ָʾ���� ����ǡ�������˵������ ��
�ٵζ�ǰ�Ƿ�Ҫ�μ�ָʾ���� ����ǡ�������˵������ ��
![]() ��ijͬѧ��ȡ5.000g�����Ԥ������������ƿ�����Ƴ�100ml��Һ����ȡ25.00ml��������Һ����1.000��10-2mol�� L-1KMnO4����Һ�ζ����ﵽ�ζ��յ�ʱ�����ı���Һ20.00ml,�����������Ԫ�ص����������� ��
��ijͬѧ��ȡ5.000g�����Ԥ������������ƿ�����Ƴ�100ml��Һ����ȡ25.00ml��������Һ����1.000��10-2mol�� L-1KMnO4����Һ�ζ����ﵽ�ζ��յ�ʱ�����ı���Һ20.00ml,�����������Ԫ�ص����������� ��
(1)MnO2 + 4H�� + 2Cl��![]() Mn2�� + Cl2�� + 2H2O
Mn2�� + Cl2�� + 2H2O
![]() (2)ƽ��ѹǿ Ũ���� ʹSiCl4 ����
(2)ƽ��ѹǿ Ũ���� ʹSiCl4 ����
![]() (3)Al��P��Cl
(3)Al��P��Cl
![]() (4)�ٷ�KMnO4��Һ��������ָʾ����
(4)�ٷ�KMnO4��Һ��������ָʾ����
![]() ��4.480%
��4.480%![]()
![]()
![]()
![]()
![]()
![]()
![]()

����:
�Ʊ����Ȼ����ԭ��ΪCl2��Si��Aװ��ΪCl2���Ʊ�װ�ã�B��Cװ��Ϊ����װ�á���B��ȥHCl������C��ŨH2SO4����ȥH2O������Cl2ͨ��ֹ��з�Ӧ������ˮ������SiCl4�������ɡ�
��1����ȡ������Ũ�����MnO2�ڼ��������·�Ӧ��
��2��g���ǽ���Һ©������ƿ�������������е�ѹǿ������ģ���������������˳�����¡�SiCl4�ķе�ܵͣ�ֻ��57.7�棬����Ӧ���¶ȴX�ٶȣ�����Ҫ�����ռ���
��3�������ʵ��������ʱ��ɷ��֣�AlCl3,FeCl3��PCl5�����������ʻ�Ӧ����Al��P��ClԪ�ء�
��4�����ڸ�����ر������Ϻ�ɫ�ģ���Fe2����Ӧʱ��������ɫ���ʶ�������Ϊָʾ�������ݷ���ʽ�����ҳ���ϵ��5Fe2��~MnO4�� ,n(Fe)= 10-2��20��10-3��5��100/25 =4��10-3mol��W (Fe)= 4��10-3��56/5 ��100% =4.48%��

 ��ĩ1�����ʽ���������ϵ�д�
��ĩ1�����ʽ���������ϵ�д�
�����Ϣ���£�
a.���Ȼ�����ˮ����ˮ�⣻
b.�������������ڸ����¾���������ֱ�ӷ�Ӧ������Ӧ���Ȼ��
c.�й����ʵ������������±���
���� | SiCl4 | BCl3 | AlCl3 | FeCl3 | PCl�±�5 |
�е�/�� | 57.7 | 12.8 | �� | 315 | �� |
�۵�/�� | -70.0 | -107.2 | �� | �� | �� |
�����¶�/�� | �� | �� | 180 | 300 | 162 |
��ش��������⣺
(1)д��װ��A�з�����Ӧ�����ӷ���ʽ____________��
(2)װ��A��g�ܵ�������____________��װ��C�е��Լ���;װ��E�е�hƿ��Ҫ��ȴ��������____________________________________��
(3)װ��E��hƿ�ռ����Ĵֲ����ͨ���������ƶ�����õ��ߴ������Ȼ��裬�����IJ������У�����Ԫ������ܻ����е�����Ԫ����____________����дԪ�ط��ţ���
(4)Ϊ�˷�������������Ԫ�صĺ������Ƚ�������Ԥ������ʹ��Ԫ�ػ�ԭ��Fe2+,����KMnO4����Һ�����������½���������ԭ�ζ�����Ӧ�����ӷ���ʽ�ǣ�5Fe2++MnO-4+8H+====5Fe3++Mn2++4H2O
�ٵζ�ǰ�Ƿ�Ҫ�μ�ָʾ����________����ǡ�������˵������__________________��
��ijͬѧ��ȡ5.000 g�������Ԥ������������ƿ�����Ƴ�100 mL��Һ����ȡ25.00 mL������Һ����1.000��10-2 mol��L-1 KMnO4����Һ�ζ����ﵽ�ζ��յ�ʱ�����ı���Һ20.00 mL�������������Ԫ�ص�����������________________��
��10�֣�����������Ϣ��ҵ����Ҫ�Ļ������ϡ�ͨ����̿�ڸ����»�ԭ���������Ƶôֹ�(������������������)���ֹ���������Ӧ�������Ȼ��裨��Ӧ�¶�450~500�棩�����Ȼ��辭�ᴿ����������ԭ�ɵøߴ��衣������ʵ�����Ʊ����Ȼ����װ��ʾ��ͼ��

�����Ϣ���£�
�����Ȼ�����ˮ����ˮ�⣻
���������������ڸ����¾���������ֱ�ӷ�Ӧ������Ӧ���Ȼ��
���й����ʵ������������±���
|
���� |
SiCl4 |
BCl3 |
AlCl3 |
FeCl3 |
PCl5 |
|
�е�/�� |
57.7 |
12.8 |
�� |
315 |
�� |
|
�۵�/�� |
��70.0 |
��107.2 |
�� |
�� |
�� |
|
�����¶�/�� |
�� |
�� |
180 |
300 |
162 |
��ش��������⣺
��1��д��װ��A�з�����Ӧ�����ӷ���ʽ ��
��2��װ��A��g�ܵ������� ��װ��C�е��Լ��� ��
װ��E�е�hƿ��Ҫ��ȴ�������� ��
��3��װ��E��hƿ�ռ����Ĵֲ����ͨ���������ƶ�����õ��ߴ������Ȼ��裬�����IJ������У�����Ԫ������ܻ����е�����Ԫ���� ����дԪ�ط��ţ���
��4��Ϊ�˷�������������Ԫ�صĺ������Ƚ�������Ԥ������ʹ��Ԫ�ػ�ԭ��Fe2��,����KMnO4����Һ�����������½���������ԭ�ζ�����Ӧ�����ӷ���ʽ�ǣ�
5Fe2����MnO4����8H�� 5Fe3����Mn2����4H2O
5Fe3����Mn2����4H2O
�ٵζ�ǰ�Ƿ�Ҫ�μ�ָʾ���� ����ǡ�������˵������
��
��ijͬѧ��ȡ5.000g�������Ԥ������������ƿ�����Ƴ�100 mL��Һ����ȡ25.00 mL������Һ����1.000��10��2 mol/L KMnO4����Һ�ζ����ﵽ�ζ��յ�ʱ�����ı���Һ20.00 mL�������������Ԫ�ص����������� ��
 www.ks5.u.com
www.ks5.u.com