题目内容
向存在大量Na+、Cl-的溶液中通入足量的NH3后,该溶液中还可能大量存在的离子组是
| A.K+、Br-、CO32- | B.Al3+、H+、MnO4- |
| C.NH4+、Fe3+、SO42- | D.Ag+、Cu2+、NO3- |
A
解析试题分析:离子间如果发生化学反应,则不能大量共存,反之是可以的。氨气溶于水生成一水合氨,溶液显碱性。A、在碱性溶液中大量Na+、Cl-、K+、Br-、CO32-能大量共存,A正确;B、首先MnO4-能氧化Cl-生成氯气,不能大量共存。其次通入氨气后H+、Al3+不能大量共存,B不正确;C、在碱性条件下Fe3+不能大量共存,C不正确;D、首先Cl-与Ag+不能大量共存,另外通入氨气后Ag+、Cu2+不能大量共存,D不正确,答案选A。
考点:考查离子共存的正误判断

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列离子方程式书写正确的是
A.铝粉投入到NaOH溶液中: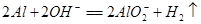 |
B.铁与盐酸反应: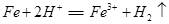 |
C.用小苏打治疗胃酸过多: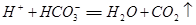 |
D.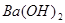 与稀 与稀 反应: 反应: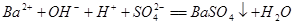 |
某溶液中含有AlO2-、SO32-、SO42-、Na+,向其中加入Na2O2后,溶液中浓度基本保持不变的离子是
| A.SO32- | B.Na+ | C.AlO2- | D.SO42- |
下列离子方程式正确的是
| A.铁跟盐酸反应:2Fe +6H+ ==2Fe3++3H2↑ |
| B.氯气与水反应:Cl2+H2O ="=" 2H++Cl+ClO- |
| C.硫酸与氢氧化钡溶液反应:Ba2++OH-+H++SO42-=BaSO4↓+ H2O |
| D.金属钠与水反应:2Na +2H2O ==2Na++2OH-+H2↑ |
下列反应的化学方程式(或离子方程式)错误的是
A.乙醛与银氨溶液反应 CH3CHO+2[Ag(NH3)2]OH  CH3COONH4+2Ag↓+3NH3+H2O CH3COONH4+2Ag↓+3NH3+H2O |
B.酯的水解反应 CH3CH2OOCCH3+H218O  CH3CH2OH+CH3CO18OH CH3CH2OH+CH3CO18OH |
| C.苯酚与氢氧化钠溶液反应 C6H5OH+OH—→ C6H5O—+H2O |
| D.醋酸溶解水垢(主要成分是碳酸钙)CO32-+CH3COOH →CO2↑+CH3COO-+H2O |
下列示意图与对应的反应情况正确的是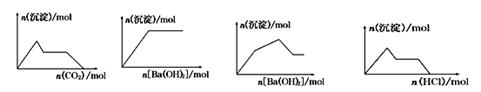
A B C D
| A.含0.01 mol KOH和0.01 mol Ca(OH)2的混合溶液中缓慢通入CO2 |
| B.NaHSO4溶液中逐滴加入Ba(OH)2溶液 |
| C.KAl(SO4)2溶液中逐滴加入Ba(OH)2溶液 |
| D.NaAlO2溶液中逐滴加入盐酸 |
常温下,在下列各组溶液中,加水稀释时c(OH-) / c(H+)值明显增大,且能大量共存的离子组是( )
① K+、Al3+、NO3-、AlO2- ② K+、Fe3+、I-、SO42-
③ Ba2+、I-、NO3-、Na+ ④ Na+、Ca2+、Al3+、 Cl-
| A.①② | B.①③ | C.②④ | D.②③ |
下列离子方程式书写正确的是
| A.澄清石灰水与少量小苏打溶液混合:Ca2+ +2OH- +2HCO3- = CaCO3↓+ CO32- + 2H2O |
| B.氯化铝溶液中加入过量的氨水:Al3+ + 4NH3·H2O = Al(OH)4-↓+ 4NH4+ |
| C.少量CO2通入苯酚钠溶液中:2C6H5O-+CO2+H2O=2C6H5OH+ CO32- |
| D.向NH4HSO4稀溶液中逐滴加入Ba(OH)2稀溶液至SO42-刚好沉淀完全:Ba2+ + 2OH- + NH4+ + H+ + SO4 2- = BaSO4↓+ NH3·H2O + H2O |
常温下,下列各组离子在指定溶液中一定能大量共存的是
| A.遇Fe(CN)63-显蓝色的溶液:Ca2+、 Cl-、ClO-、Fe3+ |
| B.水电离出c(OH-)>10-5mol/L: Mg2+、 Cl-、NO3-、Na+; |
| C.遇石蕊变红的溶液:Na+、 NH4+、NO3-、K+ |
| D.与铝反应产生大量氢气的溶液:Ba2+、 HCO3- 、l- 、Fe2+ |