题目内容
NA表示阿佛加德罗常数,下列说法正确的是
| A.常温常压下,0.1molC8H18所含有的共价键数目为2.5NA |
| B.0.1mol过氧化钠固体中含有的阴离子数为0.2NA |
| C.标准状况下2.24L三氧化硫中所含氧原子数为0.3NA |
| D.0.1mol氯气与热的氢氧化钠溶液反应时转移电子数为0.1NA |
A
试题分析:A项,0.1molC8H18中含有2.5mol共价键,即2.5NA,对
B项,1mol过氧化钠由2molNa+和1molO2-构成,故0.1mol过氧化钠固体中含有的阴离子数为0.1NA,错
C项标况下,三氧化硫为固体,错
D项氯气与热的氢氧化钠溶液反:Cl2+6NaOH=5NaCl+NaClO3+3H2O,转移的电子数为0.5NA
点评:阿伏伽德罗常数是高中化学的常考点,1mol气体在标况下的体积才为22.4L,一是气体,二是标况,两者缺一不可,此为常考考点,考生应注意。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
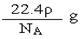
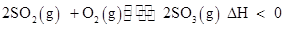 升温该平衡逆向移动,ΔH减小
升温该平衡逆向移动,ΔH减小