题目内容
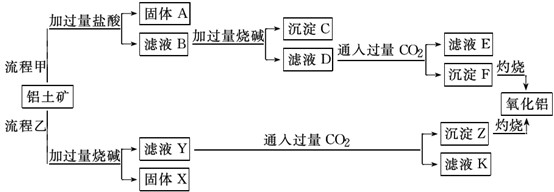
(10分)从铝土矿(主要成分是Al2O3,含SiO2、Fe2O3、MgO等杂质)中提取氧化铝的两种工艺流程如下:
请回答下列问题:
(1)流程甲通入过量CO2后生成沉淀F的离子反应方程式为______________________________________。
(2流程乙加入烧碱溶解SiO2的化学反应方程式____________________。
(3)验证滤液B含Fe3+,可取少量滤液并加入________(填试剂名称)。
(4)滤液E、K中溶质的主要成分是________(填化学式),写出该溶质的一种用途____________________。
(5)已知298 K时,Mg(OH)2的溶度积常数Ksp=5.6×10-12,取适量的滤液B,加入一定量的烧碱至达到沉淀溶解平衡,测得pH=12,则此温度下残留在溶液中的c(Mg2+)=________________。

请回答下列问题:
(1)流程甲通入过量CO2后生成沉淀F的离子反应方程式为______________________________________。
(2流程乙加入烧碱溶解SiO2的化学反应方程式____________________。
(3)验证滤液B含Fe3+,可取少量滤液并加入________(填试剂名称)。
(4)滤液E、K中溶质的主要成分是________(填化学式),写出该溶质的一种用途____________________。
(5)已知298 K时,Mg(OH)2的溶度积常数Ksp=5.6×10-12,取适量的滤液B,加入一定量的烧碱至达到沉淀溶解平衡,测得pH=12,则此温度下残留在溶液中的c(Mg2+)=________________。
(1) [Al(OH)4]-+CO2 = Al(OH)3↓+HCO3-(2分)
(2) SiO2+2NaOH===Na2SiO3+H2O(2分)
(3)硫氰化钾(或硫氰酸钾、苯酚溶液等合理答案) (2分)
(4)NaHCO3(1分) 制纯碱(或做发酵粉等合理答案)(1分)(5)5.6×10-8 mol/L(2分)
(2) SiO2+2NaOH===Na2SiO3+H2O(2分)
(3)硫氰化钾(或硫氰酸钾、苯酚溶液等合理答案) (2分)
(4)NaHCO3(1分) 制纯碱(或做发酵粉等合理答案)(1分)(5)5.6×10-8 mol/L(2分)
(1)铝土矿加入盐酸后,二氧化硅和盐酸不反应,所以A是二氧化硅。B中含有氯化铝、氯化铁、氯化镁和过量的盐酸。加入过量的烧碱后,生成氢氧化铁和氢氧化镁沉淀,即C是氢氧化铁和氢氧化镁,而D是偏铝酸钠以及过量的氢氧化钠,所以通入CO2生成沉淀F的方程式为[Al(OH)4]-+CO2 = Al(OH)3↓+HCO3-。
(2)铝土矿和烧碱反应时,氧化铁和氧化镁不反应,所以X时氧化铁和氧化镁。Y是偏铝酸钠、硅酸钠和过量的烧碱。因此二氧化硅和烧碱反应的方程式为SiO2+2NaOH===Na2SiO3+H2O。
(3)检验铁离子的试剂是KSCN溶液或苯酚。
(4)滤液D、Y和过量CO2反应后的溶液中主要含有的溶质是碳酸氢钠。碳酸氢钠常用来制纯碱(或做发酵粉等)。
(5)pH=12,则溶液中OH-浓度是0.01mol·L-1。根据溶度积常数的表达式 可知,溶液中c(Mg2+)=5.6×10-12/0.0001=5.6×10-8 mol/L。
可知,溶液中c(Mg2+)=5.6×10-12/0.0001=5.6×10-8 mol/L。
(2)铝土矿和烧碱反应时,氧化铁和氧化镁不反应,所以X时氧化铁和氧化镁。Y是偏铝酸钠、硅酸钠和过量的烧碱。因此二氧化硅和烧碱反应的方程式为SiO2+2NaOH===Na2SiO3+H2O。
(3)检验铁离子的试剂是KSCN溶液或苯酚。
(4)滤液D、Y和过量CO2反应后的溶液中主要含有的溶质是碳酸氢钠。碳酸氢钠常用来制纯碱(或做发酵粉等)。
(5)pH=12,则溶液中OH-浓度是0.01mol·L-1。根据溶度积常数的表达式
 可知,溶液中c(Mg2+)=5.6×10-12/0.0001=5.6×10-8 mol/L。
可知,溶液中c(Mg2+)=5.6×10-12/0.0001=5.6×10-8 mol/L。
练习册系列答案
相关题目
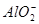 +6H2O=4Al(OH)3↓,正确的做法是
+6H2O=4Al(OH)3↓,正确的做法是