题目内容
高铁酸钠(Na2FeO4)是水处理过程中使用的一种新型净水剂,它的氧化性比高锰酸钾强,其本身在反应中被还原为Fe3+。已知制取高铁酸钠的化学方程式为:
2Fe(NO3)3+16NaOH+3Cl2===2Na2FeO4+6NaNO3+6NaCl+8H2O,回答下列问题:
(1)该反应中________得到电子,表现____________(填“氧化性”或“还原性”),Na2FeO4为________(填“氧化剂”、“还原剂”、“氧化产物”或“还原产物”)。
(2)若有1 mol Cl2参加反应,则反应中转移电子的物质的量为________。
(3)Na2FeO4之所以能净水,除了能消毒杀菌外,另一个原因是
________________________________________________________________________
________________________________________________________________________
________________________________________________________________________
________________________________________________________________________。
解析 反应物Fe(NO3)3中铁显+3价,生成物Na2FeO4中铁显+6价,Fe(NO3)3中的
Fe3+失去电子,表现还原性,而反应物Cl2中氯显0价,生成物NaCl中氯显-1价,Cl2得到电子,表现氧化性,因铁的化合价反应后升高,故Na2FeO4为氧化产物。
答案 (1)Cl2 氧化性 氧化产物 (2)2 mol (3)六价铁被还原成三价铁,三价铁水解生成氢氧化铁胶体,具有较大的表面积,能吸附杂质而沉降下来达到净水的目的

| A、钢铁制品被锈蚀主要是因为钢铁中含有碳而发生原电池反应,因此生铁炼钢时要尽可能完全除去生铁中的碳 | B、海水淡化和工业生产及生活的废水再利用,是解决缺水问题的有效途径之一 | C、高铁酸钠Na2FeO4和Cl2O都能作为净水剂,其原理完全相同 | D、液氯罐泄漏时,可将其移入水塘中,并向水塘中加入生石灰 |
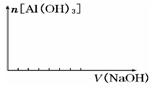
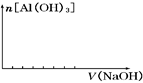
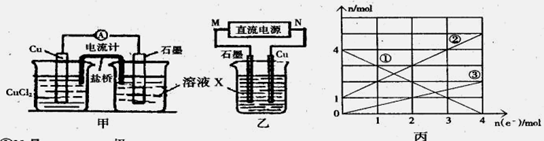

 Na2FeO4+3H2↑,则电解时阳极的电极反应式是 。
Na2FeO4+3H2↑,则电解时阳极的电极反应式是 。 2Na2FeO4+Na2O
2Na2FeO4+Na2O