题目内容
【题目】某化学兴趣小组为探究铜跟浓硫酸的反应,用下图所示装置进行有关实验。
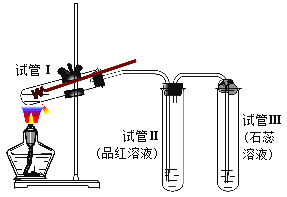
请回答下列问题:
(1)试管Ⅰ中发生反应的化学方程式为:___________________________________________。
(2)可抽动铜丝的作用是_________________________。
(3)试管Ⅱ中现象为_____________________________;可证明_____________________________________。
(4)试管Ⅲ的管口用浸有碱(NaOH溶液)的棉团塞住,其作用是___________________;
【答案】 Cu+2 H2SO4(浓) ![]() CuSO4+SO2↑+2H2O 可控制反应随时停止 品红溶液褪色 SO2具有漂白性 吸收未反应完的SO2,防止SO2污染环境。
CuSO4+SO2↑+2H2O 可控制反应随时停止 品红溶液褪色 SO2具有漂白性 吸收未反应完的SO2,防止SO2污染环境。
【解析】(1)试管Ⅰ中铜与浓硫酸在加热条件下反应生成二氧化硫,反应的化学方程式为:Cu+2H2SO4(浓)![]() CuSO4+SO2↑+2H2O,故答案为:Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O,故答案为:Cu+2H2SO4(浓)![]() CuSO4+SO2↑+2H2O;
CuSO4+SO2↑+2H2O;
(2)通过抽动铜丝,以随时中止反应,避免浪费原料、减少污染气体的产生,故答案为:可控制反应随时停止;
(3)二氧化硫具有漂白性,所以试管Ⅱ中品红溶液褪色,故答案为:品红溶液褪色;SO2具有漂白性;
(4)二氧化硫有毒,多余的气体不能直接排放,需要用氢氧化钠溶液吸收SO2气体,防止空气污染,反应的化学方程式为:SO2+2NaOH=Na2SO3+H2O,故答案为:吸收未反应完的SO2,防止SO2污染环境。

 名校课堂系列答案
名校课堂系列答案【题目】下列各组物质不能按![]() “
“![]() ” 表示反应一步完成关系转化的是
” 表示反应一步完成关系转化的是 ![]()
选项 | a | b | c |
A | SiO2 | Na2SiO3 | H2SiO3 |
B | AlCl3 | Al(OH)3 | NaAlO2 |
C | Fe | Fe(OH)3 | Fe2O3 |
D | MgCl2 | Mg(OH)2 | MgO |
A. A B. B C. C D. D