题目内容
向含有Fe2+、I-、Br-的溶液中通入适量氯气,溶液中各种离子的物质的量变化如图所示。有关说法不正确的是( )
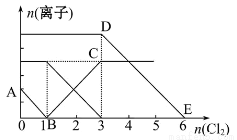
A.线段BC代表Fe3+物质的量的变化情况
B.原混合溶液中c(FeBr2)=6 mol/L
C.当通入Cl2 2 mol时,溶液中已发生的离子反应可表示为:2Fe2++2I-+2Cl2=2Fe3++I2+4Cl-
D.原溶液中n(Fe2+)∶n(I-)∶n(Br-)=2∶1∶3
B
【解析】还原性强弱顺序为:I->Fe2+>Br-,所以Cl2最先氧化I-,然后氧化Fe2+,最后氧化Br-。图中AB线段表示I-的变化情况,氧化I-需氯气1 mol,则I-为2 mol;BC线段表示Fe3+的变化情况,氧化Fe2+需氯气2 mol,则Fe2+为4 mol;DE线段表示Br-的变化情况,氧化Br-需氯气3 mol,则Br-为6 mol。当通入Cl2 2 mol时,氧化的I-和Fe2+均为2 mol,所以C中的离子方程式是正确的。因不知溶液的体积,则B错误。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目