题目内容
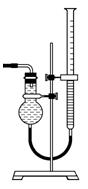
下图是制取和收集某气体的实验装置,可用于
A.用Zn粒与稀HCl反应制H2 B.用Na2O2与H2O反应制O2
C.用Cu与稀HNO3反应制NO D.用MnO2与浓HCl反应制Cl2
A 由实验装置可知,制取的气体不需要加热,且是用向下排空气法收集,即密度小于空气的,A项制取H2符合条件.O2、Cl2不能用向下排空气法,且D中的方法需要加热,C中生成的NO不能用排空气法,因2NO+O2![]() 2NO2,只能用排水集气法,故正确答案为A.
2NO2,只能用排水集气法,故正确答案为A.

 阅读快车系列答案
阅读快车系列答案I. 实验室里用二氧化锰和浓盐酸加热制取氯气,该反应的离子方程式为: MnO2+4H++2Cl—![]() Mn2++Cl2↑+2H2O,也可以利用反应:
Mn2++Cl2↑+2H2O,也可以利用反应:
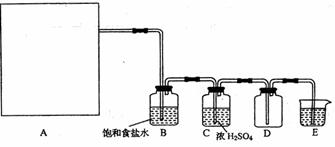
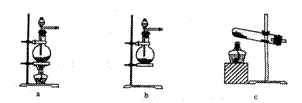
2KMnO4+16HCl(浓) 2KCl+2MnCl2+5Cl2↑+8H2O制取并收集纯净、干燥的氯气,部分装置如图所示:
|
(1)若以KMnO4和浓盐酸为原料制取氯气,请根据反应原理从下图中选择合适的制气装置 (填代号)。
|
(2)装置B的作用是 。
(3)E中的试剂可选用 (填代号)。
A.NaOH溶液 B.Na2CO3溶液 C.NaCl溶液 D.水
(4)某学生通过下列两种方式制取氯气:
①用8.7gMnO2与足量浓盐酸反应制取Cl2
②用含14.6gHCl的浓盐酸与足量MnO2反应制取Cl2
这两种方式产生Cl2的量的关系是 。
A.①多 B.②多 C.①②一样多
II.现欲用碳酸钙固体和稀盐酸反应制取CO2气体,请回答下列问题:
(1)写出发生反应的离子方程式 ;
|
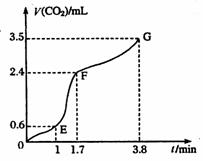
[V(CO2)]与时间(t)的关系如图
所示,试分析判断OE段、EF段、
FG段反应速率[分别用![]() (OE)、
(OE)、![]()
(EF)、![]() (FG)表示]的大小关系
(FG)表示]的大小关系
;比较OE段和EF
段,说明EF段速率变化的主要原因
应该是 。

 _________________________________。
_________________________________。 _________________________。
_________________________。 ;
;
 图所示量气装置由干燥管、乳胶管和50 mL滴定管改造后组装而成,此处所用滴定管是________(填“酸式”或“碱式”)滴定管。
图所示量气装置由干燥管、乳胶管和50 mL滴定管改造后组装而成,此处所用滴定管是________(填“酸式”或“碱式”)滴定管。 会导致所测气体的体积__________(填“偏大”、“偏小”或“无影响”)。
会导致所测气体的体积__________(填“偏大”、“偏小”或“无影响”)。