题目内容
(1)某化学小组的同学在学习了NaHCO3和Na2CO3的有关知识后,进行如下实验:在两支试管中分别加入3 mL、4 mol·L-1稀盐酸,将两个各装有0.3 g NaHCO3或Na2CO3粉末的小气球分别套在两支试管口.将气球内的NaHCO3或Na2CO3同时倒入试管中,观察到现象如下:

①试管中(填产生沉淀或气体及反应速率等相关现象)________.
②盛________的试管中气球变得更大,大小气球(包含试管)体积之比约为(填最简单整数比)________;
③甲同学用手触摸试管,发现盛NaHCO3粉末的试管变冷,而盛Na2CO3的试管温度有升高.由此他得出:不管其状态如何,NaHCO3和HCl反应为吸热反应,而Na2CO3和HCl反应为放热反应.类似如中和热,甲同学写出了下列热化学方程式:
HCO3-(aq)+H+(aq)=H2O(l)+CO2(g);△H>0
CO32-(aq)+2H+(aq)=H2O(l)+CO2(g);△H<0
甲下结论的方法是否正确________(填“正确”或“不正确”)
(2)为研究是吸热还是放热反应,继续进行了下列实验(每次实验各做3次平行实验,取平均值):
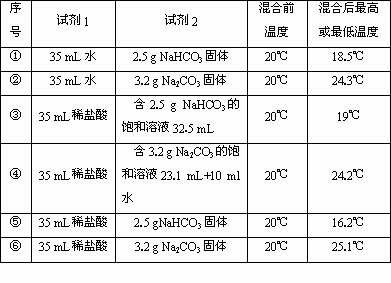
请你帮助填写相关内容:
①该研究报告的题目是《________》;
②该实验中所用的仪器除试管、药匙(或V型纸槽)、气球、玻璃棒、烧杯、量筒、保温瓶外,还需要的仪器名称为________和________;通过上述实验可得出五条结论:
a:NaHCO3的溶解是________(“吸热”或“放热”)过程;
b:Na2CO3的溶解是________(“吸热”或“放热”)过程;
c:NaHCO3的饱和溶液和盐酸的反应是________(“吸热”或“放热”)反应;
d:Na2CO3的饱和溶液和盐酸的反应是________(“吸热”或“放热”)反应;
e:NaHCO3固体与稀盐酸反应的反应热是________(填a→d的字母)的热效应之和.
解析:
|
(1)①答案:碳酸氢钠放出气泡快 解析:NaHCO3和Na2CO3与稀盐酸的反应,前者反应速率块,故反应开始时,盛碳酸氢钠的试管中放出气泡快,产生的CO2气体多,气球体积先变大. ②答案:碳酸氢钠、53∶42 解析:由关系式NaHCO3~HCl~CO2,Na2CO3~2HCl~CO2可知,NaHCO3、Na2CO3分别与3 mL 4 mol·L-1盐酸完全反应时,需二者的质量分别为:1.008 g、0.636 g,故均为0.3 g的NaHCO3、Na2CO3不足,二者全反应掉.产生CO2的体积比约为(0.3/84)∶(0.3/106)=53∶42. ③答案:不正确 解析:同学仅通过感官的冷、热得出“不管其状态如何,NaHCO3和HCl反应为吸热反应,而Na2CO3和HCl反应为放热反应”的结论是不正确的.因为NaHCO3、Na2CO3固体与稀盐酸反应的反应热是通过NaHCO3、Na2CO3固体溶解的热效应和其饱和溶液与盐酸反的应热效应之和来计算的. (2)①答案:关于碳酸氢钠与碳酸钠与盐酸反应热效应的研究 解析:该实验是研究物质反应的热量变化的,所以该研究报告的题目是《关于碳酸氢钠与碳酸钠与盐酸反应热效应的研究》. ②答案:温度计、托盘天平、吸热放热吸热、放热a、c 解析:该实验中所用的仪器有试管、药匙、气球、玻璃棒、烧杯、量筒、保温瓶、温度计、托盘天平等.通过分析上述表中的数据,知:NaHCO3的溶解是吸热过程;Na2CO3的溶解是放热过程;NaHCO3的饱和溶液和盐酸的反应是吸热反应;Na2CO3的饱和溶液和盐酸的反应是放热反应.NaHCO3固体与稀盐酸反应的反应热是NaHCO3的溶解和NaHCO3的饱与溶液和盐酸的反应二者的热效应之和. |

 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案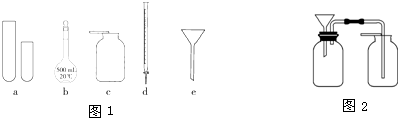
(1)指导教师要求同学们写出仪器的名称,甲同学书写的答案如下表,请你找出其中的错误,将改正后的名称填写在下表中(若正确,则此空不需要填写).
| 仪器编号 | a | b | c | d | e |
| 名称 | 试管 | 溶量瓶 | 集气瓶 | 碱式滴定管 | 普通漏斗 |
| 改正的名称 |
①
(3)d仪器在使用前必须检查是否漏水,检查漏水的操作是
(4)丙同学想用如图2所示装置用大理石和稀盐酸反应制取CO2.老师指出,这需要太多的稀盐酸,会造成浪费.该同学选用了上面的一种仪器,加在装置中,解决了这个问题.请你把该仪器画在图中合适的位置.
某化学小组的同学到实验室学习.如图1在实验桌上摆有下列仪器:
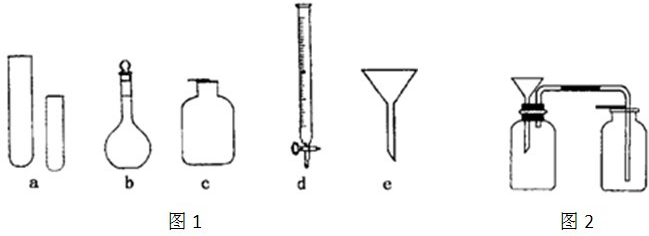
(1)指导教师要求同学们写出仪器的名称,甲同学书写的答案如下表,请你找出其中的错误,将改正后的名称填写在下表中(若正确,则该空不需要填写).
| 仪器编号 | a | b | c | d | e |
| 名称 | 试管 | 溶量瓶 | 集气瓶 | 碱式滴定管 | 普通漏斗 |
| 改正的名称 | ______ | ______ | ______ | ______ | ______ |
①______;
②______.
(3)丙同学想用图2装置以大理石和稀盐酸反应制取CO2.教师指出,这需要太多的稀盐酸,造成浪费.该同学选用了上面的一种仪器,加在装置上,解决了这个问题.请你把该仪器画在图中合适的位置.
某化学小组的同学到实验室学习。在实验桌上摆有下列仪器:

(1)指导教师要求同学们写出仪器的名称,甲同学书写的答案如下表,请你找出其中的错误,将改正后的名称填写在下表中(若正确,则该空不需要填写。)
| 仪器编号 | a | b | c | d | e |
| 名称 | 试管 | 容量瓶 | 集气瓶 | 碱式滴定管 | 普通漏斗 |
| 改正的名称 |
(2)关于e的用途,乙同学说:组成防倒装置。你还能说出其他两种用途吗?
① ;
② 。
(3)丙同学想用下图装置以大理石和稀盐酸反应制取CO2。教师指出,这需要太多的稀盐酸,造成浪费。该同学选用了上面的一种仪器,加在装置上,解决了这个问题。请你把该仪器画在图中合适的位置。

(08广东实验中学三模)(7分)某化学小组的同学到实验室学习。在实验桌上摆有下列仪器:
 |
(1)指导教师要求同学们写出仪器的名称,甲同学书写的答案如下表,请你找出其中的错误,将改正后的名称填写在下表中(若正确,则该空不需要填写。)
仪器编号 | a | b | c | d | e |
名称 | 试管 | 溶量瓶 | 集气瓶 | 碱式滴定管 | 普通漏斗 |
改正的名称 |
|
|
|
|
|
(2)关于e的用途,乙同学说:组成防倒吸装置。你还能说出
① ;② 。
(3)丙同学想用下图装置以大理石和稀盐酸反应制取CO2。
 教师指出,这需要太多的稀盐酸,造成浪费。该同学选用了上面的一种仪器,加在装置上,解决了这个问题。请你把该仪器画在图中合适的位置。
教师指出,这需要太多的稀盐酸,造成浪费。该同学选用了上面的一种仪器,加在装置上,解决了这个问题。请你把该仪器画在图中合适的位置。
