题目内容
下列离子方程式,书写正确的是( )
A.氯气溶于水:Cl2+H2O=2H++Cl-+ClO-
B.硫酸铝溶液中加入足量氨水:Al3++4OH-=[Al(OH)4]-
C.FeSO4溶液与稀硝酸反应:3Fe2++NO3—+4H+=3Fe3++NO↑+2H2O
D.碳酸氢铵和足量氢氧化钠溶液反应:NH4++OH-=NH3·H2O
 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案a、b、c、d、e、f、g、h为8种由短周期元素构成的微粒,它们都含有10个电子,其结构特点如下:
微粒代码 | a | b | c | d | e | f | g | h |
单核 | 单核 | 双核 | 多核 | 单核 | 多核 | 多核 | 多核 | |
0 | +1 | -1 | 0 | +2 | +1 | 0 | 0 |
其中b的离子半径大于e的离子半径,d是由极性键构成的四原予极性分子;c与f可形成两个共价型g分子,h是5原子分子。下列说法不正确的是( )
A. d的水溶液显碱性 B. b对应最高价氧化物对应水化物的碱性比e强
C. h具有可燃性 D. e相应的元素的单质与g微粒在加热条件下也不能反应
铁及其化合物在日常生活、生产中应用广泛,研究铁及其化合物的应用意义重大。请回答下列问题:
(1)已知高炉炼铁过程中会发生如下反应:
FeO(s)+CO(g) Fe(s)+CO2(g) K1 ΔH1=a kJ·mol?1
Fe(s)+CO2(g) K1 ΔH1=a kJ·mol?1
3Fe2O3(s)+CO(g) 2Fe3O4(s)+CO2(g) K2 ΔH2=b kJ·mol?1
2Fe3O4(s)+CO2(g) K2 ΔH2=b kJ·mol?1
Fe3O4(s)+CO(g) 3FeO(s)+CO2(g) K3 ΔH3=c kJ·mol?1
3FeO(s)+CO2(g) K3 ΔH3=c kJ·mol?1
①Fe2O3(s)+3CO(g) 2Fe(s)+3CO2(g) ΔH=_____kJ·mol?1(用含a、b、c的代数式表示)。
2Fe(s)+3CO2(g) ΔH=_____kJ·mol?1(用含a、b、c的代数式表示)。
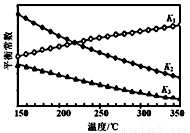
②上述反应对应的平衡常数K1、K2、K3随温度变化的曲线如图所示。则a_________b,(填“>”、“<”或“=”),理由是_________________。
(2)铁的氧化物粉末和Al粉在镁条的引燃下可以发生铝热反应,下列反应速率(v)和温度(T)的关系示意图中与铝热反应最接近的是________。

(3)铁等金属可用作CO与H2反应的催化剂:CO(g)+3H2(g) CH4(g)+H2O(g)
CH4(g)+H2O(g)
ΔH<0。在T℃,将l mol CO和3 mol H2加入2 L的密闭容器中。实验测得n(CO)随时间的变化如下表:
t/min | 0 | 10 | 20 | 30 | 40 | 50 |
n(CO)/mol | 1.0 | 0.70 | 0.45 | 0.25 | 0.10 | 0.10 |
①下列能判断该反应达到平衡的标志是______(填序号)。
a.容器内压强不再发生变化 b.混合气体的密度不再发生变化
c.v正(CO)=3v逆(H2) d.混合气体的平均相对分子质量不再发生变化
②在0~20 min内v (H2)=______;在T℃时该反应的平衡常数K=_________。
③下图表示该反应中CO的转化率与温度、压强的关系。图中压强P1、P2、P3由高到低的顺序是_________。





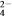


 的叙述错误的是( )
的叙述错误的是( )
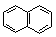 )的衍生物,且取代基都在同—个苯环上;
)的衍生物,且取代基都在同—个苯环上; (R为烃基)。根据已有知识并结合相关信息,写出以ClCH2CH2CH2Cl和
(R为烃基)。根据已有知识并结合相关信息,写出以ClCH2CH2CH2Cl和 为原料制备
为原料制备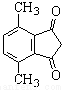 的合成路线流程图(无机试剂可任选)。
的合成路线流程图(无机试剂可任选)。 是原子能工业的一种重要原料,可作为核燃料和核武器的裂变剂。下列关于Pu-239的说法不正确的是
是原子能工业的一种重要原料,可作为核燃料和核武器的裂变剂。下列关于Pu-239的说法不正确的是 互为同位素 B.
互为同位素 B.  为两种不同核素
为两种不同核素