题目内容
在碱性条件下能够大量共存,而在强酸性条件下却能发生氧化还原反应的离子组是( )
A. |
| B.K+、Na+、ClO-、Fe2+ |
C. |
D.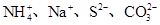 |
C
B、D项中分别含Fe2+、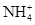 ,碱性条件下不能够大量共存,A项在酸性条件下不能发生氧化还原反应,C项中
,碱性条件下不能够大量共存,A项在酸性条件下不能发生氧化还原反应,C项中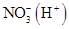 能够氧化I-。故C项符合题意
能够氧化I-。故C项符合题意
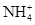 ,碱性条件下不能够大量共存,A项在酸性条件下不能发生氧化还原反应,C项中
,碱性条件下不能够大量共存,A项在酸性条件下不能发生氧化还原反应,C项中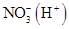 能够氧化I-。故C项符合题意
能够氧化I-。故C项符合题意
练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
 HSO3-+H+的电离常数Ka=1×10-2mol·L-1,则该温度下NaHSO3水解反应的平衡常数Kb=________mol·L-1,若向NaHSO3溶液中加入少量的I2,则溶液中
HSO3-+H+的电离常数Ka=1×10-2mol·L-1,则该温度下NaHSO3水解反应的平衡常数Kb=________mol·L-1,若向NaHSO3溶液中加入少量的I2,则溶液中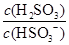 将________(填“增大”、“减小”或“不变”)。
将________(填“增大”、“减小”或“不变”)。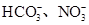 。已知该溶液可与Al2O3反应,则:
。已知该溶液可与Al2O3反应,则: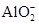 生成,则原溶液中一定含有_______,可能含有大量的_______。
生成,则原溶液中一定含有_______,可能含有大量的_______。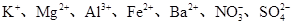 、
、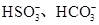 、I-和Cl-,取该溶液进行如下实验:
、I-和Cl-,取该溶液进行如下实验: