题目内容
钛(Ti)因为具有神奇的性能越来越受到人们的关注。常温下钛不和非金属、强酸反应,红热时,却可以与常见非金属单质反应。钛是航空、军事、电力等方面的必需原料。地壳中有一种含钛矿石称金红石(TiO2),目前大规模生产钛的方法是:
(1)第一步:金红石(TiO2)、炭粉混合,在高温条件下通入Cl2制取TiCl4和一种可燃性气体。该反应的化学方程式为___________________,该反应的还原剂是___________。
(2)第二步:在氩气的气氛中,用过量的镁在加热条件下与TiCl4反应制得金属钛。
写出此反应的化学方程式____________________。
如何由上述所得产物获取金属钛?简述步骤并写出有关反应的化学方程式:________。
(1)第一步:金红石(TiO2)、炭粉混合,在高温条件下通入Cl2制取TiCl4和一种可燃性气体。该反应的化学方程式为___________________,该反应的还原剂是___________。
(2)第二步:在氩气的气氛中,用过量的镁在加热条件下与TiCl4反应制得金属钛。
写出此反应的化学方程式____________________。
如何由上述所得产物获取金属钛?简述步骤并写出有关反应的化学方程式:________。
(1)TiO2+2C+2Cl2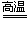 TiCl4+2CO;C
TiCl4+2CO;C
(2)TiCl4+2Mg =Ti+2MgCl2;加入足量的盐酸除去过量的镁,过滤,并用蒸馏水洗涤固体可得到金属钛,Mg+2HCl=MgCl2+H2↑
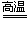 TiCl4+2CO;C
TiCl4+2CO;C (2)TiCl4+2Mg =Ti+2MgCl2;加入足量的盐酸除去过量的镁,过滤,并用蒸馏水洗涤固体可得到金属钛,Mg+2HCl=MgCl2+H2↑

练习册系列答案
 一线名师提优试卷系列答案
一线名师提优试卷系列答案
相关题目