题目内容
m molC2H2跟n molH2在密闭容器内反应,当其达到平衡时,生成p molC2H6。将平衡混合气体完全燃烧,所需O2物质的量是( )
| A.(3m+n)mol | B.(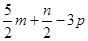 )mol )mol |
| C.(3m+n+2p)mol | D.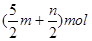 |
D
试题分析:无论平衡时生成多少C2H4,其充分燃烧时所需O2的量总是跟原来C2H2和H2的量有关。所以就用mmolC2H2与nmolH2计算燃烧时所需的氧气即可。则根据乙炔和氢气的燃烧方程式可知,需要氧气的物质的量是2.5mmol+0.5nmol,答案选D。
点评:该题是基础性试题的考查,难度不大,试题基础性强,侧重对学生能力的培养。该题的关键是利用好原子守恒,有利于培养学生的灵活应变能力和创新思维能力。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目