题目内容
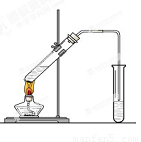
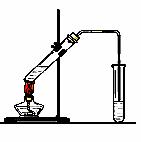
实验室可以用如图所示仪器连接起来,制备纯净的CO2并测定其相对分子质量.

现用含有少量硫化亚铁的大理石和盐酸反应制备CO2气体,实验步骤如下:
(1)将橡皮塞B塞在烧瓶A的瓶口,并用橡皮筋套在烧瓶的瓶颈处以标记橡皮塞所塞入瓶颈的深度,准确称其质量为m1 g.
(2)连接制备和净化气体的装置,其连接顺序是:________接________,________接________,________接________,,________接________.
(3)将导管G插入烧瓶A中用向________(填“上”或“下”)排空气法收集二氧化碳气体.检验二氧化碳气体已经充满烧瓶的方法是________.若经检验,二氧化碳气体已经充满烧瓶,迅速用橡皮塞塞好烧瓶瓶口,并称其质量为m2 g.
(4)将瓶口橡皮塞取下,向烧瓶中注水至标记线,再将水小心地倒入量筒,测量出水的体积为V1 mL;将该体积换算成标准状况时的体积为V2 mL.请写出二氧化碳的相对分子质量的计算式:________.若不将气体净化和干燥,所测定的二氧化碳相对分子质量的数值将会________(填“偏高”或“偏低”),其理由是________.
(5)若没有现成的CO2气体发生器,请你选用如图中的部分仪器,装配成一个简易并且能随用、随关、随停的CO2气体发生装置.应选用的仪器是________(填编号).

解析:
|
【解答】(2)g,a,b,c,d,e,f,h(或g,c,d,a,b,e,f,h);(3)上,用燃着的木条放在瓶口,若火焰熄灭,则证明CO2已经充满;(4) 【巧解导析】因反应后产生的CO2中含HCl,H2S,H2O(气)等杂质,需要除去,其操作规律一般是先进行溶液的除杂操作,后进行干燥.其原因是气体通过溶液时(浓H2SO4除外)将带出水蒸气,干燥剂可除去这些水蒸气.故装置的连接顺序为g→a→b→c→d→e→f→h或g→c→d→a→b→e→f→h.又因m1=瓶重+空气,m2=瓶重+CO2,故m2-m1为瓶中CO2与空气的质量差.由题意知瓶中气体的物质的量= |
提示:
|
【巧解点悟】解实验题的关键要弄清实验的目的及原理,根据实验的目的答题.此类题若不仔细分析,没有形成一定的分析思路则很易做错. |

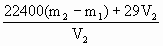 ,偏低,因为含有H2S,HCl,H2O等杂质气体的相对分子质量均小于CO2的相对分子质量;(5)acde
,偏低,因为含有H2S,HCl,H2O等杂质气体的相对分子质量均小于CO2的相对分子质量;(5)acde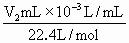 ,所以有等式
,所以有等式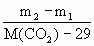 =
=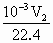 ,所以M(CO2)=
,所以M(CO2)=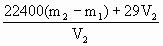 .若不除杂质,则CO2中有H2S,HCl,H2O式量均小于CO2,故会使测定数值偏低.寻找启普发生器的替代品,不妨先画出草图,看能否具有启普发生器的优点.
.若不除杂质,则CO2中有H2S,HCl,H2O式量均小于CO2,故会使测定数值偏低.寻找启普发生器的替代品,不妨先画出草图,看能否具有启普发生器的优点.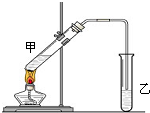 俗话说,“陈酒老醋特别香”,其原因是酒在储存过程中生成了有香味的乙酸乙酯,在实验室里我们也可以用如图所示的装置来模拟该过程.请回答下列问题:
俗话说,“陈酒老醋特别香”,其原因是酒在储存过程中生成了有香味的乙酸乙酯,在实验室里我们也可以用如图所示的装置来模拟该过程.请回答下列问题: