题目内容
关于钢铁腐蚀与防护的说法不正确的是
| A.钢铁的吸氧腐蚀和析氢腐蚀的负极反应式均为:Fe-2e-= Fe2+ |
| B.钢铁发生吸氧腐蚀时,正极反应式为:O2+2H2O+4e-= 4OH- |
| C.地下钢管连接镁块是采用牺牲阳极的阴极保护法 |
| D.用外加电流的阴极保护法防止钢铁腐蚀时,钢铁接电源的正极 |
D
试题分析:A、发生腐蚀时,活泼的金属作负极,不如负极活泼的金属或导电的非金属作正极,所以铁作负极,氧气作正极,负极失电子变成离子进入溶液,负极反应为Fe-2e-= Fe2+;B、正极上得电子发生还原反应,故吸氧腐蚀时正极反应O2+2H2O+4e-= 4OH-C、牺牲阳极的阴极保护法:其原理是利用原电池原理对金属进行防护,其方法是:将被保护的金属作为原电池的正极,将比被保护金属活泼的另一种金属作为原电池的负极,镁比铁活泼作为阳极保护阴极铁,故C正确;D、外加电流的阴极保护法:其原理是利用电解池原理对金属进行防护,其方法是:将被保护的金属作为电解池的阴极,用惰性电极作为辅助阳极,两者均存在于电解质溶液中,接上外加直流电源,钢铁应作为阴极连接电源负极,故D错误。

练习册系列答案
相关题目

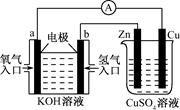
 3Zn(OH)2+2Fe(OH)3+4KOH,按要求回答下列问题:
3Zn(OH)2+2Fe(OH)3+4KOH,按要求回答下列问题: