��Ŀ����
X��Y��Z���������ֶ�����Ԫ����ɵ�������ǵ�ÿ�������о�����l8�����ӣ������Ϣ���±���ʾ(��������ʾ��Ӧ����Ϣ��ȥ)��
�ش��������⣺
��1��X����������ƽ���������ӵ����ģ��Ϊ ����X�Ļ�ѧʽΪ .
����X�Ļ�ѧʽΪ .
��2��Y�Ļ�ѧ����������ȷ���� ��
a�����ȶ��� b�������� c�������� d����ԭ��
��3��Z�Ļ�ѧʽ����H2A��ʾ����һ������Z����ͨ��0��05mol��L-1CuSO4��Һ�У�����ǡ����ȫ��Ӧ����֪Ksp(CuA)=6��0��10-36������������Һ����ı仯����
�ٷ�Ӧ����Һ��pH= ��
������Ӧ����Һ��c(A2-)=2��0��10-30mol��L-1������Һ��c(Cu2+)= mol��L-1��
��4����һ������Z����ͨ��NaOH��Һ�У���������Һ����μ���ϡ������������������������HCl�����ʵ����Ĺ�ϵ��ͼ��ʾ(����������ܽ��HCl�Ļӷ�)��

��O����Һ���������ʵĻ�ѧʽΪ ��
����֪a����Һ�ʼ��ԣ�����Һ�����ӵ����ʵ���Ũ���ɴ�С��˳���� ��
| ������ | X | Y | Z |
| �����к��е�ԭ�Ӹ��� | / | 4 | / |
| Ħ��������g��mol-l | 32 | 34 | / |
�ش��������⣺
��1��X����������ƽ���������ӵ����ģ��Ϊ
 ����X�Ļ�ѧʽΪ .
����X�Ļ�ѧʽΪ .��2��Y�Ļ�ѧ����������ȷ���� ��
a�����ȶ��� b�������� c�������� d����ԭ��
��3��Z�Ļ�ѧʽ����H2A��ʾ����һ������Z����ͨ��0��05mol��L-1CuSO4��Һ�У�����ǡ����ȫ��Ӧ����֪Ksp(CuA)=6��0��10-36������������Һ����ı仯����
�ٷ�Ӧ����Һ��pH= ��
������Ӧ����Һ��c(A2-)=2��0��10-30mol��L-1������Һ��c(Cu2+)= mol��L-1��
��4����һ������Z����ͨ��NaOH��Һ�У���������Һ����μ���ϡ������������������������HCl�����ʵ����Ĺ�ϵ��ͼ��ʾ(����������ܽ��HCl�Ļӷ�)��

��O����Һ���������ʵĻ�ѧʽΪ ��
����֪a����Һ�ʼ��ԣ�����Һ�����ӵ����ʵ���Ũ���ɴ�С��˳���� ��
��1��N2H4����2��acd����3����1����3.0��10-6mol��L-1��
��4����Na2S��NaOH����c(Na+)��c(Cl��)��c(HS��)��c(OH��)��c(H+)��c(S2-)��
��4����Na2S��NaOH����c(Na+)��c(Cl��)��c(HS��)��c(OH��)��c(H+)��c(S2-)��
�����������������֪��X��Y��Z���������ֶ�����Ԫ����ɵ�������ǵ�ÿ�������о�����l8�����ӣ�X����������ƽ��������X���ӵĽṹģ���жϣ�XΪN2H4��Y�����к��е�ԭ�Ӹ���Ϊ4����Է�������Ϊ34 ����YΪH2O2��Z�Ļ�ѧʽ����H2A��ʾ����ZΪH2S����1��������������֪��X�Ļ�ѧʽΪN2H4����2��YΪH2O2����ѧ����Ϊa�����ȶ���c�������� d����ԭ�ԣ�ѡacd����3��ZΪH2S����һ������H2S����ͨ��0��05mol��L-1CuSO4��Һ�У�����ǡ����ȫ��Ӧ������ͭ���������ᡣ�ٷ�Ӧ����Һ��������Ũ��Ϊ0.1mol��L-1��pH=1��������Ӧ����Һ��c(S2-)=2��0��10-30mol��L-1������Ksp(CuS)=c(Cu2+)c(S2-)=6��0��10-36���㣬����Һ��c(Cu2+)=3.0��10-6mol��L-1����4���������ͼ���Ϸ�ӦNa2S+HCl==NaHS+NaCl��NaHS+HCl==NaCl+H2S����֪����O����Һ���������ʵĻ�ѧʽΪNa2S��NaOH������ͼ���֪��a����ҺΪNaCl��NaHS���Һ���Ȼ��Ƶ�Ũ�ȴ������⻯�Ƶ�Ũ�ȣ���Һ�ʼ��ԣ���������ӵ�ˮ��̶ȴ��ڵ���̶ȣ�����Һ�����ӵ����ʵ���Ũ���ɴ�С��˳����c(Na+)��c(Cl��)��c(HS��)��c(OH��)��c(H+)��c(S2-)��

��ϰ��ϵ�д�
 ��У����ϵ�д�
��У����ϵ�д�
�����Ŀ
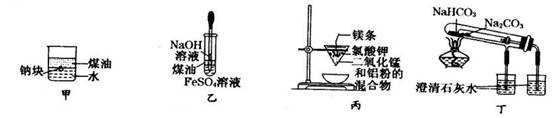
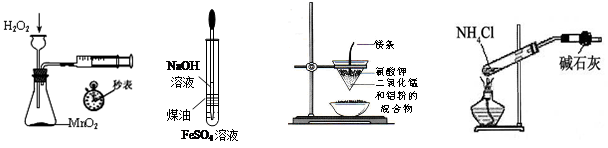
 ���������й����ʵ��ƶϲ���ȷ���� (����)��
���������й����ʵ��ƶϲ���ȷ���� (����)��